Cho 39 gam kim loại Kali vào 362 gam nước thu được dung dịch X. Nồng độ phần trăm của chất tan trong dung dịch X là
A. 10,00%.
B. 14,00%.
C. 9,75%.
D. 13,96%
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH: \(K+H_2O\rightarrow KOH+\dfrac{1}{2}H_2\uparrow\)
Ta có: \(n_K=\dfrac{1,95}{39}=0,05\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}n_{KOH}=0,05\left(mol\right)\\n_{H_2}=0,025\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow C\%=\dfrac{0,05\cdot56}{1,95+12,1-0,025\cdot2}\cdot100\%=20\%\)
\(\Rightarrow\) Chọn B

nK = \(\dfrac{39}{39}\) = 1 (mol)
PTHH: 2K + 2H2O→ 2KOH + H2
nH2 =\(\dfrac{1}{2}\).nK = 0,5 mol; nKOH = nK = 1 mol;
mdung dịch = mK + mH2O – mH2
=39 + 362 – 0,5.2
= 400 (gam)
C%KOH=\(\dfrac{m_{KOH}}{mddsau}\).100%C%KOH= \(1,\dfrac{56}{400}\).100%= 14%.
Chọn C
PTHH: 2K + 2H2O→ 2KOH + H2
nH2 =1212.nK = 0,5 mol; nKOH = nK = 1 mol;
mdung dịch = mK + mH2O – mH2
=39 + 362 – 0,5.2
= 400 (gam)
C%KOH=mKOHmddsau.100%C%KOH=mKOHmddsau.100% = 1.56400.100%1.56400.100% = 14%.
B

nNa = 6.9 : 23 = 0.3 mol
4Na + O2 ->2 Na2O
mol : 0.3 -> 0.15
Na2O + H2O -> 2NaOH
mol : 0.15 -> 0.3
mdd = 0.15 x 62 + 140.7 = 150g
C% NaOH = 0.3x40: 150 x 100% = 8%

Đáp án A
Gọi n là hoá trị của M; x là số mol của M
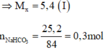
Phương trình hoá học:
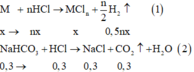
Dung dịch X thu được gồm NaCl: 0,3 mol; MCn: x mol; HCl dư

Tổ hợp (I) và (II) ta được:
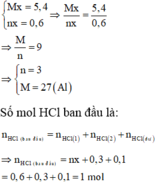
Số mol các khí thu được theo (1), (2) là:
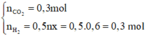
Nồng độ phần trăm của NaCl trong dung dịch X là:
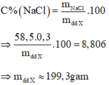
Mặt khác, ta có:
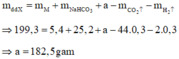
Nồng độ phần trăm dung dịch HCl ban đầu là:
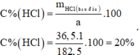

Đáp án C.
K + H2O → KOH + 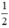 H2
H2
Số mol K: nK = 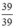 = 1(mol)
= 1(mol)
Số mol KOH: nKOH = nK = 1(mol)
Khối lượng KOH là mKOH = 56.1 = 56 (g)
Số mol H2: nH2 = 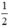 nK= 0,5(mol)
nK= 0,5(mol)
Khối lượng dung dịch là mdd = 39 + 362 – 0,5.2 = 400 (g)
Nồng độ C%KOH = 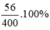 = 14%
= 14%

\(n_K=\frac{5,85}{15}=0,15(mol)\\ K+H_2O \to KOH +\frac{1}{2}H_2\\ n_{KOH}=n_K=0,15(mol)\\ n_{H_2}=\frac{1}{2}.n_K=\frac{1}{2}.0,15=0,075(mol)\\ m_{dd}=5,85+100-(0,075.2)=105,7(g)\\ C\%=\frac{0,15.56}{105,7}.100=7,95\%\)

a)
\(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right)\)
PTHH: 2Na + 2H2O --> 2NaOH + H2
0,2-------------->0,2--->0,1
=> Chất tan trong dd X là NaOH
mNaOH = 0,2.40 = 8 (g)
mdd sau pư = 4,6 + 59,6 - 0,1.2 = 64 (g)
=> \(C\%=\dfrac{8}{64}.100\%=12,5\%\)
b)
PTHH: CuO + H2 --to--> Cu + H2O
0,1------>0,1
=> mCu = 0,1.64 = 6,4 (g)

a)
\(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right)\)
PTHH: 2Na + 2H2O --> 2NaOH + H2
0,2-------------->0,2--->0,1
=> Chất tan trong dd X là NaOH
mNaOH = 0,2.40 = 8 (g)
mdd sau pư = 4,6 + 59,6 - 0,1.2 = 64 (g)
=> \(C\%=\dfrac{8}{64}.100\%=12,5\%\)
b)
PTHH: CuO + H2 --to--> Cu + H2O
0,1------>0,1
=> mCu = 0,1.64 = 6,4 (g)
Đáp án B
m C t = m K O H = 1.56 = 56 gam.
m d d = m K L + m n ư ớ c - m k h í = 39 + 362 – 0,5.1 = 400 gam.