Cho hỗn hợp X gồm Fe, FeO, Fe3O4, Fe2O3 tan hoàn toàn trong dung dịch HNO3 thu được 0,4 mol Fe(NO3)3 và 5,6 lít hỗn hợp khí gồm NO2 và NO (đktc). Vậy số mol HNO3 đã phản ứng là
A. 1,45 mol
B. 1,4 mol
C. 1,35 mol
D. 1,2 mol
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Quy đổi hỗn hợp về Fe và O. Đặt nFe = a và nO = b
+ Vì HNO3 dư và nFe(NO3)3 = 0,4 mol ⇒ nFe = a = 0,4 mol
+ Áp dụng bảo toàn e ta có: 3nFe = 2nO + 3nNO
⇒ nO = 0,3 mol ⇒ m = 0,4×56 + 0,3×16 = 27,2 gam

Dung dịch Y chứa Fe3+ (a); Fe2+ (b), Cl- (0,88) và nH+ dư = 4nNO = 0,88 (mol)
Bảo toàn điện tích: 3a + 2b + 0,08 = 0,88 (1)
nAgCl = 0,88 => nAg = 0,07 (mol)
Bảo toàn electron: b = 0,03.2 + 0,07 (2)
Từ (1) và (2) => a = 0,18 và b = 0,13 (mol)
Quy đổi hỗn hợp thành Fe ( 0,31 mol) ; O ( u mol) và NO3- ( v mol). Trong Z, đặt nN2O = x => nNO2 = 0,2 – x (mol)
=> 0,31.56 + 16u + 62v = 27,04 (3)
Bảo toàn nguyên tố N:
v + 0,04 = 2x + (0,12 –x) (4)
nH+ pư = 0,88 + 0,04 – 0,08 = 0,84
=> 10x + 2( 0,12 –x) + 2u = 0,84 (5)
Từ (3), (4), (5) => u = 0,14 ; v = 0,12 ; x = 0,04
nFe(NO3)2 = v/2 = 0,06 (mol)
Đặt k, 3h, 2h, h lần lượt là số mol Fe, FeO, Fe3O4, Fe2O3
Bảo toàn Fe: => 0,06 + k + 11h = 0,31 (6)
Bảo toàn O : => 14h = u = 0,14 (7)
Từ (6) và (7) => k = 0,14 (mol); h = 0,01 (mol)
Số mol hỗn hợp = 0,06 + k + 6h = 0,26
=> %nFe = 0,14/0,26 = 53,85%
Gần nhất với 54%
Đáp án A

Đáp án C
Bảo toàn Cl : nHCl = nAgCl = 0,88 mol
,mkết tủa = mAgCl + mAg(nếu có) = 133,84g => nAg = 0,07 mol = nFe2+
=> dung dịch Y có Fe2+ và Fe3+ ; H+ dư ,Cl- (không có NO3-)
3Fe2+ + 4H+ + NO3- -> 3Fe3+ + NO + 2H2O
Fe2+ + Ag+ -> Fe3+ + Ag
=> nH+ dư = 4nNO = 0,08 mol ; nFe2+(Y) = 3nNO + nAg = 0,13 mol
Bảo toàn điện tích : 2nFe2+ + 3nFe3+ + nH+ = nCl- => nFe3+ = 0,18 mol
Gọi số mol Fe : x ; FeO : 3y ; Fe3O4 : 2y ; Fe2O3 : y ; Fe(NO3)2 : z
=> nX = x + 6y + z
=> Qui về : x mol Fe ; 5y mol FeO ; 3y mol Fe2O3 ; z mol Fe(NO3)2
=> mX = 56x + 840y + 180z = 27,04
Bảo toàn Fe : x + 11y + z = 0,13 + 0,18 = 0,31 mol
,nH+ pứ bđ = 2nH2O => nH2O = ½ (0,88 + 0,04 – 0,08) = 0,42 mol
Bảo toàn khối lượng : mX + mHCl + mHNO3 = mion muối Y + mKhí + mH2O
=> mKhí = mNO2 + mN2O = 5,44g và nNO2 + nN2O = 0,12
=> nNO2 = 0,08 ; nN2O = 0,04 mol
Bảo toàn N : 2nFe(NO3)2 + nHNO3 = 2nN2O + nNO2 => nFe(NO3)2 = z = 0,06 mol
=>x = 0,14 ; y = 0,01
=> nX = 0,26 mol
=> %nFe(X) = 53,85%
=>C

Đáp án C
Phân tích kết tủa:
0,88 mol Cl → 0,88 mol AgCl → 133,84 gam kết tủa còn 0,07 mol Ag nữa.
AgNO3 + dung dịch Y → 0,02 mol NO chứng tỏ trong Y chứa 0,08 mol H+.
Thêm nữa, kết tủa có Ag → chứng tỏ trong Y có Fe2+ → Y không chứa NO 3 - .
Rõ hơn quan sát sơ đồ:
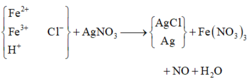
Theo đó, bảo toàn Ag có 0,95 mol AgNO3 → có 0,31 mol Fe(NO3)3.
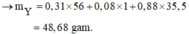
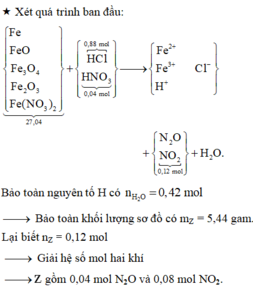
→ Bảo toàn nguyên tố N có số mol Fe(NO3)2 trong X là 0,06 mol.
Nhìn 27,04 gam X gồm 0,31 mol Fe + 0,12 mol NO3 + ? mol O → ? = 0,14 mol.
Lại có tỉ lệ FeO : Fe3O4 : Fe2O3 = 3:2:1
→ viết gộp cụm: 3FeO.2Fe3O4.1Fe2O3 = Fe11O14.
→ từ 0,14 mol O suy ra có 0,01 mol Fe11O14.
→ đọc ra có 0,03 mol FeO + 0,02 mol Fe3O4 + 0,01 mol Fe2O3.
→ nFe có trong X ban đầu = 0,31 - 0,11 - 0,06 = 0,14 mol
→ yêu cầu %nFe có trong hỗn hợp X
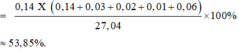
Chọn đáp án A.
BTNT.N => nHNO3 = 0,4 × 3 + 5,6/22,4 = 1,45 mol.