Một dung dịch có chứa 0,02 mol NH4+, x mol Fe3+, 0,01 mol Cl- và 0,02 mol SO42-. Khi cô cạn dung dịch này thu được lượng muối khan là:
A. 2,635 gam
B. 3,195 gam
C. 4,315 gam
D. 4,875 gam
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Theo định luật bảo toàn điện tích: 0,02.3+ 0,03.2=x + 2y
mmuối= 0,02.27+ 0,03.56 + 35,5.x+ 96.y=7,23
Suy ra x=0,06; y=0,03
Ta có: 2 cation: 0,02 mol Al3+, 0,03 mol Fe2+ và 2 anion: 0,06 mol Cl-, 0,03 mol SO42-
Suy ra 2 muối là FeCl2 và Al2(SO4)3

Chọn B.
Bảo toàn điện tích: ![]()
Tương đương: 3.0,2 + 2.0,25 = 2a + 0,5 ⇒ a = 0,3 mol.
Bảo toàn khối lượng: mmuối = 0,2.27 + 0,3.96 + 0,25.24 + 0,5.35,5 = 57,95 gam.

Đáp án B
0,1.3 + 0,1.2 = 0,2.2 +![]() = 0,1
= 0,1
Bảo toàn khối lượng mmuối = 0,1.27 + 0,1.64 + 0,2.96 + 0,1.35,5 = 31,85g

0,1.3 + 0,1.2 = 0,2.2 + n Cl - → n Cl - = 0,1
Bảo toàn khối lượng → mmuối = 0,1.27 + 0,1.64 + 0,2.96 + 0,1.35,5 = 31,85g
Đáp án B

Chọn B
Bảo toàn điện tích có:
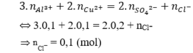
Bảo toàn khối lượng có:
mmuối = ∑mion = 0,1.27 + 0,1.64 + 0,2.96 + 0,1.35.5 = 31,85 (gam).

Bảo toàn điện tích :
\(3a+2b=0.08+0.12=0.2\left(1\right)\)
\(m_{Muối}=56a+56b+0.08\cdot35.5+0.12\cdot62=15.32\left(g\right)\)
\(\Leftrightarrow a+b=0.09\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.02,b=0.07\)
\(Fe^{2+}+Ag^+\rightarrow Fe^{3+}+Ag\)
\(0.07......0.07.....................0.07\)
\(m\downarrow=0.07\cdot108+0.08\cdot143.5=19.04\left(g\right)\)

Đáp án B
Bảo toàn điện tích: nCl- = 3nAl3+ + 2nCu2+ - 2nSO42- = 0,1
mmuối =mAl3+ + mCu2+ + mSO42- + mCl- = 31,85g

Bảo toàn điện tích: 2x = 0,1 + 0,2.3 – 0,4 = 0,3 → x = 0,15 mol
![]()
→ m = 0,1.39 + 0,2.56 + 0,4.62 + 0,15.96 = 54,3 gam
Đáp án B
Đáp án B
Theo định luật bảo toàn điện tích: 0,02.1+ 3.x= 0,01.1+ 0,02.2
Suy ra x=0,01 mol
Khối lượng muối khan thu được khi cô cạn dung dịch là:
0,02.18+ 0,01.56+ 0,01.35,5+ 0,02.96= 3,195 gam