Hoà tan m gam Na kim loại vào nước thu được dung dịch X. Trung hoà dung dịch X cần 100ml dung dịch H2SO4 1M. Giá trị m đã dùng là
A. 6,9 gam
B. 4,6 gam
C. 9,2 gam
D. 2,3 gam
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
n OH - = 2 n H 2 = 0 , 48 ⇒ 1 2 dung dịch C có n OH - = 0 , 48 2 = 0 , 24
Dung dịch D có: n H + = 2 n H 2 SO 4 + n HCl = 2 a + 4 a = 6 a
Vì trung hòa 1/2 dung dịch C bằng dung dịch D nên 6a=0,24 óa=0,04
Vậy m = m kl + m SO 4 2 - + m Cl -
= 1 2 m X + 96 a + 35 , 5 . 4 a = 18 , 46 ( gam )

đáp án B
Ta có nH2=0.24 nên nOH-=0.48 toàn bộ OH- phản ứng với H+ được thay bằng các gốc axit tạo muối nên nH+ của H2SO4=2/(2+4) *0.24=0.08
nên nSO4=0.04,n Cl=0.16
=> m muôi=17.88+0.04*96+0.16*35.5=27.4

Đáp án C
Các phản ứng: Na + H2O → NaOH + ½ H2
2NaOH + H2SO4 → Na2SO4 + 2H2O
nH2SO4 = 0,1.1 = 0,1 mol
Theo các phản ứng: nNa = nNaOH = 2nH2SO4 = 0,2 mol
=> mNa = m = 23.0,2 = 4,6g

\(Na+HCl \to NaCl+\frac{1}{2}H_2\\ n_{Na}=2n_{H_2}=2.0,4=0,8(mol)\\ m_{Na}=0,8.23=18,4(g)\)

Bắt đầu xuất hiện kết tủa n H C l = n N a O H ( d u ) = 0 , 1 S ố m o l H C l s a u k h i p h ả n ứ n g v ớ i N a O H n H C l ( 1 ) = 0 , 2 - 0 , 1 = 0 , 1 ; n H C l ( 2 ) = 0 , 6 - 0 , 1 = 0 , 5
Do khi cho vào 200ml hoặc 600ml HCl thì đều thu được cùng một lượng kết tủa nên ở TN1 kết tủa chưa tan, ở TN2 kết
tủa tan 1 phần
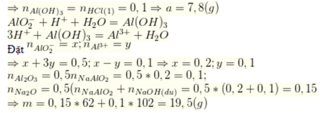

Đáp án A
Từ giả thiết suy ra : Ở TN2 đã có hiện tượng hòa tan kết tủa. Còn ở TN1 thì có thể có hiện tượng hòa tan kết tủa hoặc chưa. Ta đặt :
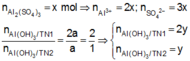
● Nếu cả TN1 và TN2 đều có hiện tượng hòa tan kết tủa, áp dụng bảo toàn điện tích cho các dung dịch sau phản ứng, ta có :
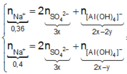
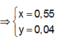
![]() thỏa mãn
thỏa mãn
Suy ra : ![]()
● Nếu TN1 chưa có hiện tượng hòa tan kết tủa, áp dụng bảo toàn điện tích cho các dung dịch sau phản ứng, ta có :
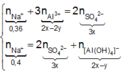
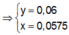
![]() (loại)
(loại)
Đáp án : B
Na -> NaOH + H2SO4
=> nNa = nNaOH = 2nH2SO4 = 0,2 mol
=> m = 4,6g