Thể tích dung dịch NaOH 1M để tác dụng hoàn toàn với 0,05 mol khí clo ở điều kiện thường là: (Giả thiết thể tích dung dịch thay đổi không đáng kể)
A. 100ml
B. 50ml
C. 500ml
D. 200ml
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Cl_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
\(2NaOH+Cl_2\rightarrow NaCl+NaClO+H_2O\)
2 mol 1 mol 1mol 1mol 1 mol
0,1 0,05 0,05 0,05 0,05
\(V_{NaOH}=\dfrac{0,1}{1}=0,1\left(l\right)\)
\(CM_{NaCl}=\dfrac{0,05}{0,1}=0,5M\)
\(CM_{NaClO}=\dfrac{0,05}{0,1}=0,5M\)

Ta có: \(n_{Cl_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PT: \(Cl_2+2NaOH\rightarrow NaCl+NaClO+H_2O\)
____0,2_______0,4______0,2______0,2 (mol)
\(\Rightarrow V_{NaOH}=\dfrac{0,4}{4}=0,1\left(l\right)\)
\(C_{M_{NaCl}}=C_{M_{NaClO}}=\dfrac{0,2}{0,1}=2\left(M\right)\)

Số mol Cl2 = 1,12 : 22,4 = 0,05 mol
Phương trình hóa học:
Cl2 + 2NaOH -> NaCl + NaClO + H2O.
Phản ứng: 0,05 0,1 0,05 0,05
Dung dịch sau phản ứng có 2 chất tan là NaCl và NaClO đều có 0,05 mol; Vdd = 0,1 lít.
CM(NaCl) = CM(NaClO) = = 0,5 M
Theo đề ta có PTHH:
\(2NaOH+Cl_2\rightarrow NaCl+NaClO+H_2O\)
theo pt:2(mol)__________________________>: 1(mol)
Theo đề, \(n_{Cl_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
Theo pt: \(n_{NaOH}=2n_{Cl_2}=2.0,05=0,1\left(mol\right)\)
\(\Rightarrow V_{NaOH}=0,1.1=0,1\left(M\right)\)
Có 2 chất sau phản ứng là NaCl và NaClO.
theo pt, \(n_{NaCl}=n_{Cl_2}=0,05\left(mol\right);n_{NaClO}=n_{NaCl}=0,05\left(mol\right)\)
\(\Rightarrow C_{MNaCl}=C_{MNaClO}=\dfrac{0,05}{0,1}=0,5\left(M\right)\)

a) Phương trình hóa học của phản ứng:
b) Theo pt (1): nCl2 = nMnCl2 = nMnO2 = 0,8 mol
Theo pt (2): nNaCl = nNaClO = nCl2 = 0,8 mol
nNaOH pư = 2. nCl2 = 2. 0,8 = 1,6 mol
⇒ nNaOH dư = 2 - 1,6 = 0,4 mol
Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM (NaCl) = CM (NaClO) = CM(MnCl2) = 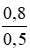
CM (NaOH)dư = 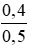
tích cho mình nha![]()

PTHH: \(CaCl_2+Na_2CO_3\rightarrow CaCO_3\downarrow+2NaCl\)
a+b) Ta có: \(n_{CaCl_2}=0,1\cdot2=0,2\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{CaCO_3}=0,2\left(mol\right)\\n_{NaCl}=0,4\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{CaCO_3}=0,2\cdot100=20\left(g\right)\\C_{M_{NaCl}}=\dfrac{0,4}{0,1+0,2}\approx1,33\left(M\right)\end{matrix}\right.\)
c) PTHH: \(CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\)
Theo PTHH: \(n_{HCl}=2n_{CaCO_3}=0,4\left(mol\right)\) \(\Rightarrow m_{ddHCl}=\dfrac{0,4\cdot36,5}{10\%}=146\left(g\right)\)
a.PTHH:CaCl2+Na2CO3--->CaCO3+2NaCl
Ta có:nCaCl2=0,2
=>nCaCO3=nCaCl2=0,2(mol)=>mCaCO3(kết tủa)=100.0,2=2(g)
b.Vdd=100+200=300(ml)=0,3(l)
CM Nacl=(2.0,2)/0,3=4/3(M)(Đề cho 2 chất td vừa đủ nên dd sau pứ chỉ có NaCl)
c.CaCO3+2HCl--->CaCl2+CO2+H2O
nHCl(cần dùng)=2.0.2=0,4(mol)=>mHCl=36,5.0,4=14,6(g)
=>mddHCl=14,6/10%=146(g)

– Số mol KMnO4 = 0,2 (mol); số mol KOH = 2 (mol)
– Phương trình phản ứng:
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
0,2 0,5
* Ở điều kiện nhiệt độ thường:
Cl2 + 2KOH → KCl + KClO + H2O
0,5 1,0 0,5 0,5
– Dư 1,0 mol KOH
CM (KCl) = CM (KClO) = 0,5 (M); CM (KOH dư) = 1 (M)
* Ở điều kiện đun nóng trên 700C:
3Cl2 + 6KOH → 5KCl + KClO3 + 3H2O
0,5 1,0 5/6 1/6
– Dư 1,0 mol KOH
CM (KCl) = 5/6 (M); CM (KClO3) = 1/6 (M); CM (KOH dư) = 1 (M).

\(n_{Cl_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(2NaOH+Cl_2\rightarrow NaCl+NaClO+H_2O\)
\(0.4...........0.2..........0.2.........0.2\)
\(V_{dd_{NaOH}}=\dfrac{0.4}{4}=0.1\left(l\right)\)
\(C_{M_{NaCl}}=\dfrac{0.2}{0.1}=2\left(M\right)\)
\(C_{M_{NaClO}}=\dfrac{0.2}{0.1}=2\left(M\right)\)

a) 2NaOH + Cl2 --> NaCl + NaClO + H2O
b) \(n_{Cl_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
PTHH: 2NaOH + Cl2 --> NaCl + NaClO + H2O
0,1<----0,05--->0,05----->0,05
=> \(V_{ddNaOH}=\dfrac{0,1}{1}=0,1\left(l\right)\)
c)
\(\left\{{}\begin{matrix}C_{M\left(NaCl\right)}=\dfrac{0,05}{0,1}=0,5M\\C_{M\left(NaClO\right)}=\dfrac{0,05}{0,1}=0,5M\end{matrix}\right.\)
Chọn đáp án A
2NaOH + C l 2 → NaClO + NaCl + H 2 O
n N a O H = 2 n C l 2 = 2. 0,05 = 0,1 mol
⇒ V N a O H = 0,1 : 1 = 0,1 lít = 100ml