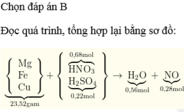
Cho 23,52 gam hỗn hợp X gồm Mg, Fe, Cu vào 200ml dung dịch HNO3 3,4M. Khuấy đều thấy thoát ra khí NO (sản phẩm khử duy nhất), trong dung dịch còn dư một kim loại chưa tan hết; đổ tiếp từ từ dung dịch Y (H2SO4 5M) vào, chất khí trên lại thoát ra cho đến khi kim loại vừa tan hết thì cần vừa hết 44ml, thu được dung dịch Y. Lấy 1/2 dung dịch Y, cho dung dịch NaOH dư vào, lọc lấy kết tủa, nung trong không khí đến khối lượng không đổi được chất rắn Z nặng 15,6 gam. Số mol Fe có trong hỗn hợp X là:
A. 0,06
B. 0,12
C. 0,24
D. 0,36



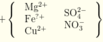




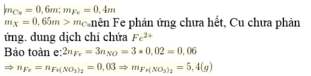
Đáp án B
nMg = a ; nFe =b ; nCu = c
⇒mX =24a+ 56b + 64c =23,52 (1)
nH+ = 0,2 . 3,4 + 0,044 .5.2 = 1,12
Do lần đầu, 1 kim loại dư nên Cu sẽ dư, dung dịch Y có: Mg2+, Cu2+, Fe2+
Ở lần hai, khi thêm H2SO4, do Cu có tính khử mạnh hơn Fe2+ nên khi Cu tan hết thì Fe2+ vẫn không phản ứng nên dung dịch Y cuối cùng sẽ có: Mg2+ , Cu2+ ; Fe2+
nH+ = 8/3 nMg2+ + 8/3 nFe2+ + 8/3 nCu2+ ⇒ 8/3 a + 8/3 b + 8/3 c = 1,12 (2)
mOxit = mMgO + mFe2O3 + mCuO ⇒ 40a +80b + 80c =15,6 .2 = 31,2 (3)
Từ (1), (2), (3) ⇒ a = 0,06; b=0,12 ; c =0,24 ⇒ nFe = 0,12 mol.