Cho m gam Fe vào 400 ml dung dịch chứa Cu(NO3)2 0,3M và AgNO3 0,6M. Sau khi các phản ứng xảy ra hoàn toàn, thu được gam hỗn hợp kim loại. Giá trị của m là
A. 17,36.
B. 11,20.
C. 10,08.
D. 16,80.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


![]()
![]()


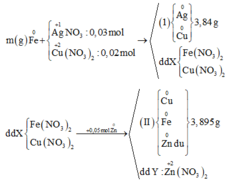
Từ sơ đồ phản ứng ta thấy Fe từ số oxi hóa 0 vẫn về 0
=> ne( Ag+, Cu2+ nhận) = ne ( Zn nhường)
Mà ∑ ne ( Ag+, Cu2+ nhận) = 0,03.1 + 0,02.2 = 0,07 < ne ( Zn nhường) = 0,1 (mol)
=> Zn còn dư sau phản ứng
=> nZn pư = ½ ne nhận = ½. 0,07 = 0,035 (mol)
=> nZn dư = 0,05 – 0,035 = 0,015 (mol)
mFe + mAg bđ + mCu bđ + mZn dư = mAg+Cu (I) + mCu + Fe + Zn (II)
=> mFe = mAg+Cu (I) + mCu + Fe + Zn (II) - ( mAg bđ + mCu bđ + mZn dư )
=> mFe = 3.84 + 3,895 – (0,03.108 + 0,02.64 + 0,015. 65)
mFe = 2,24 (g)
Đáp án B

Chọn đáp án B
Có 0,2.(0,15 + 0,1.2) = 0,07 mol nitrat trong suốt quá trình phản ứng, và như thế theo tiêu chí kim loại càng mạnh càng sót lại trước tiên thì dung dịch Y chỉ còn ion của kẽm khi lượng được đưa vào X lên tới 3,25/65 = 0,05 mol nên có 0,035 mol Zn2+ trong Y.
Bảo toàn khối lượng phần kim loại
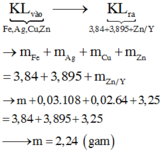

Đáp án A
![]()
↔ 0,05 mol => cuối cùng Y cho 0,035 mol Z n ( N O 3 ) 2
Bảo toàn khối lượng lần 1: ![]() = 7,26 gam
= 7,26 gam
Bảo toàn khối lượng lần 2: => m = 7,26 + 3,84 - 0,03.170 - 0,02.188 = 2,240 gam

Đáp án A
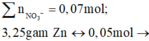 cuối cùng Y cho 0,035 mol
Z
n
(
N
O
3
)
2
cuối cùng Y cho 0,035 mol
Z
n
(
N
O
3
)
2
Bảo toàn khối lượng lần 1: mchất tan trong X
![]()
Bảo toàn khối lượng lần 2||

Đáp án : D
nMg = 0,1 ; nFe = 0,19 mol
Thứ tự phản ứng :
Mg + 2Ag+ -> Mg2+ + 2Ag
Fe + 2Ag+ -> Fe2+ + 2Ag
Fe + Cu2+ -> Fe + Cu
=> Kết tủa gồm : Ag : 0,3 mol ; Cu : 0,14 mol
=> m = 41,36g