Lấy 9,9 gam kim loại M có hoá trị không đổi đem hoà vào HNO3 loãng dư thu được 4,48 lít hỗn hợp khí X ( ở ĐKTC) gồm hai khí NO và N2O, tỉ khối của khí X đối với H2 bằng 18,5. Vậy kim loại M là
A. Zn
B. Al
C. Mg
D. Ni
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Mhh khí=37g/mol
=>mhh khí=37.0,2=7,4g
nhh khí=0,2 mol
Gọi nNO=x mol nN2O=y mol
=>x+ y=0,2 mol
Và 30x+44y=7,4=>x=y=0,1 mol
N+5 +3e =>N+2
0,3 mol<=0,1 mol
2N+5. +2.4e =>2N+1
0,8 mol<=0,2 mol
Tổng n e nhận=1,1 mol=n e nhường
GS kl M hóa trị n
M =>M+n. +ne
1,1/n mol<= 1,1 mol
=>1,1M=9,9n=>M=9n=>chọn n=3=>M=27 Al

Đáp án D
Gọi n là số oxi hóa của M trong sản phẩm tạo thành.
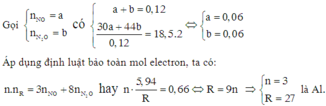

Đáp án B
n H 2 = 0 , 1 ; n NO = 0 , 4 . Gọi n là hóa trị của M.
Căn cứ vào 4 đáp án ta có 2 trường hợp:
+) M là kim loại đứng trước H trong dãy hoạt động hóa học. Khi đó cả M và Fe có phản ứng với dung dịch HCl. Vì hóa trị của M không đổi nên sự chênh lệch về số electron trao đổi trong hai lần thí nghiệm là do sắt có hai mức hóa trị là II và III.
Áp dụng định luật bảo toàn mol electron:
- Khi hòa tan hỗn hợp vào dung dịch HCl, ta có: 2 n Fe + n . n M = 2 n H 2
- Khi hòa tan hỗn hợp vào dung dịch HNO3, ta có: 3 n Fe + n . n M = 3 n NO
Trừ hai vế của hai phương trình cho nhau, ta được:
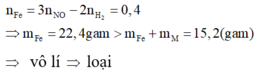
+) M là kim loại đứng sau H và trước Pt trong dãy hoạt động hóa học. Khi đó M không phản ứng được với dung dịch HCl và phản ứng được với dung dịch HNO3. Áp dụng định luật bảo toàn mol electron:
- Khi hòa tan hỗn hợp vào dung dịch HCl, ta có:


Đặt nA = x, nB = y.
Xét phản ứng 2, nCl- = 0,6 mol => nNO3- = 0,6 mol
Ta có 6m + 1,32 = 0,6.62 => m = 5,76
=> 2a + 3b = 0,6 mol
MA . x + MB . y = 5,76
Thử 4 đáp án => Mg và Al
=> Đáp án A

Đặt nN2O= x mol; nN2= y mol
Ta có nhhY= x+y= 1,12/ 22,4= 0,05 mol
mhhY=44x + 28y= 0,05.18.2
Giải hệ trên được x= 0,025 và y= 0,025
nZn= 0,3 mol= nZn(NO3)2
Quá trình cho e:
Zn→ Zn2++ 2e (1)
0,3→ 0,6 mol
Quá trình nhận e:
2NO3-+ 10e+ 12H+ → N2 + 6H2O (2)
0,25 ← 0,025 mol
2NO3-+ 8e+ 10H+ → N2O + 5H2O (3)
0,2 ← 0,025 mol
Tổng số mol e nhận ở (2) và (3) là ne nhận= 0,25+ 0,2= 0,45 mol <0,6 mol
Do đó còn xảy ra quá trình nhận e: ne nhận ở (4)= 0,6- 0,45= 0,15mol
NO3-+ 8e+ 10H+ → NH4++ 3H2O (4)
0,15 → 0, 01875 mol
Dung dịch X chứa 0,3 mol Zn(NO3)2 và 0,01875 mol NH4NO3
→m=0,3.189+ 0,01875.80=58,2 gam
Đáp án B
Chọn đáp án B
Ta có:
Vậy