Cho 6,8 gam hỗn hợp X gồm Zn và Fe vào 325ml dung dịch C u S O 4 0,2M, sau khi phản ứng hoàn toàn, thu được dung dịch và 6,96 gam hỗn hợp kim loại Y. Khối lượng Fe bị oxi khử bởi ion C u 2 + là:
A. 1,4 gam
B. 4,2 gam
C. 2,1 gam
D. 2,8 gam
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


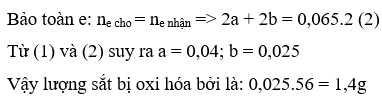

Δm = 6,96 – 6,8 = 0,16g
Zn + Cua2+ → Zn2+ + Cu
x
Fe + Cu2+ → Zn2+ + Cu
y
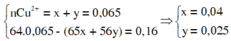
→ mFe bị oxi hóa = 0,025.56 = 1,4g
Đáp án A

Đáp án A
![]()
→ cuối cùng Y cho 0,035 mol Z n ( N O 3 ) 2
Bảo toàn khối lượng lần 1:
![]() = 7,26 gam
= 7,26 gam
Bảo toàn khối lượng lần 2:
![]()
= 2,240 gam

\(n_{Cu\left(NO_3\right)_2}=0,5.0,2=0,1\left(mol\right)\)
\(n_{NO_3^-}=0,1.2=0,2\left(mol\right)\)
\(n_{Cu^{2+}}=0,1\left(mol\right)\)
\(n_{HCl}=n_{H^+}=0,5.1,8=0,9\left(mol\right)\)
\(n_{NO}=\dfrac{n_{H^+}}{4}=\dfrac{0,9}{4}=0,225\left(mol\right)\)
Sau phản ứng thu được hỗn hợp kim loại \(\Rightarrow\) Cu và Fe \(\Rightarrow\) \(Fe^{2+}\)
Bảo toàn e:
\(2n_{Fe.pứ}=3n_{NO}+2n_{Cu^{2+}}\)
\(\Rightarrow n_{Fe.pứ}=0,4375\left(mol\right)\)
Có: \(a-m_{Fe.pứ}+m_{Cu}=m_{hh.kl}=0,5\)
\(\Leftrightarrow a-0,4375.56+64.0,1=0,5\\ \Rightarrow a=18,6\)