Sục 8,96 lit khí CO2 (đktc) vào dung dịch chứa 0,25 mol Ca(OH)2 . Khối lượng kết tủa thu được là
A. 25 gam
B. 10 gam
C. 12 gam
D. 40 gam
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án C
Quy quá trình thành: CO2 + 0,2 mol Ba(OH)2 + Ca(OH)2 dư → 49,4g ↓
⇒ nCaCO3 = (49,4 - 0,2 × 197) ÷ 100 = 0,1 mol. Bảo toàn nguyên tố Cacbon:
nCO2 = nBaCO3 + nCaCO3 = 0,2 + 0,1 = 0,3 mol ⇒ chọn C.

Đáp án C
Quy quá trình thành: CO2 + 0,2 mol Ba(OH)2 + Ca(OH)2 dư → 49,4g ↓
⇒ nCaCO3 = (49,4 - 0,2 × 197) ÷ 100 = 0,1 mol. Bảo toàn nguyên tố Cacbon:
nCO2 = nBaCO3 + nCaCO3 = 0,2 + 0,1 = 0,3 mol ⇒ chọn C.

Đáp án C.
Số mol CO2 là: 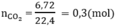
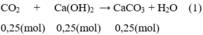
Theo pt (1): nCO2 = nCa(OH)2 = 0,25 mol
nCO2 (dư ) = 0,3 – 0,25 = 0,05 (mol)
Xảy ra phản ứng:
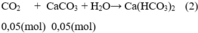
Theo pt(2): nCaCO3 pư = nCO2 = 0,05 mol
Như vậy CaCO3 không bị hòa tan là: 0,25 – 0,05 = 0,2(mol)
Khối lượng kết tủa thu được là m = 0,2. 100 = 20(g)

Đáp án D
Lượng CO 2 tham gia phản ứng và lượng Ba ( OH ) 2 ở hai thí nghiệm đều bằng nhau, nhưng ở TN1 thu được lượng kết tủa ít hơn ở TN2. Suy ra ở TN1 kết tủa đã bị hòa tan một phần. Dựa vào tính chất của đồ thị ở TN1 suy ra :
n CO 2 = 2 n Ba ( OH ) 2 - n BaCO 3 = ( 2 a - 0 , 1 ) mol
Đồ thị biểu diễn sự biến thiên lượng kết tủa theo lượng CO 2 ở TN1 và TN2 :
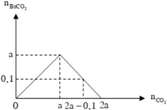
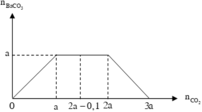
Dựa vào 2 đồ thị, ta thấy a < 2a - 0,1 < 2a nên ở TN2 kết tủa đạt cực đại. Suy ra :
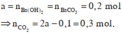
Vậy V = 6,72 lít và a = 0,2 mol

\(n_{CO_2}=0,12\left(mol\right);n_{Ca\left(OH\right)_2}=0,1\left(mol\right)\Rightarrow n_{OH^-}=0,2\left(mol\right)\\ Tacó:\dfrac{n_{OH^-}}{n_{CO_2}}=1,67\\ \Rightarrow Tạo2muốiCaCO_3vàCa\left(HCO_3\right)_2\\ Đặt:\left\{{}\begin{matrix}n_{CaCO_3}=x\left(mol\right)\\n_{Ca\left(HCO_3\right)_2}=y\left(mol\right)\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}x+2y=0,12\left(BTNT\left(C\right)\right)\\x+y=0,1\left(BTNT\left(Ca\right)\right)\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}x=0,08\\y=0,02\end{matrix}\right.\\ \Rightarrow m_{CaCO_3}=0,08.100=8\left(g\right)\)
Chọn B