Đem nung 6,7 gam hỗn hợp 2 muối CaCO 3 và XCO 3 có tỉ lệ số mol là 1:2 đến khối lượng không đổi, thấy khối lượng chất rắn giảm đi 3,3 gam. Dẫn toàn bộ lượng khí sinh ra qua bình đựng 2,5 lít dung dịch nước vôi trong 0,02M. Xác định kim loại X
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


n Ca OH 2 = 0,02 x 2,5 = 0,05 mol
CO 2 + Ca OH 2 → CaCO 3 + H 2 O
0,05 0,05 0,05 (mol)
Số mol CO 2 dư : 0,075 - 0,05 = 0,025 (mol) nên có phản ứng
CO 2 + CaCO 3 + H 2 O → Ca HCO 3 2
0,025 0,025 0,025 (mol)
Dung dịch thu được có 0,025 mol Ca HCO 3 2
C M Ca HCO 3 2 = 0,025/0,25 = 0,01M

nCO2=0.35
nOH-=0.4
OH- + CO2 -------> HCO3-
0.4 0.3
0.05 0.35
0.35 0.05HCO3- + OH- --------> CO3(2-) + H20
0.3 0 0.05
mBaCo3=9.85
đáp án B

n F e : n F e 2 O 3 = 1 : 2 56 n F e + 160 n F e 2 O 3 = 37 , 6 g
⇒ n F e = 0 , 1 m o l n F e 2 O 3 = 0 , 2 m o l
⇒ m c h a t r a n = m F e 2 O 3 = 40 g
=> Chọn đáp án A.
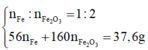
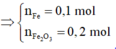
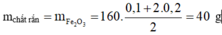

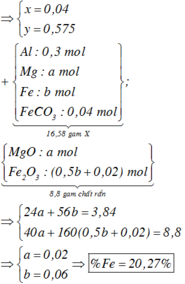

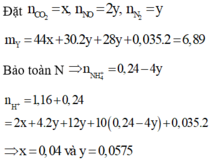

Khối lượng chất rắn giảm đi là khối lượng khí CO 2 bay ra
n CO 2 = 3,3/44 = 0,075 mol
Phương trình hoá học của phản ứng:
CaCO 3 → t ° CaO + CO 2
a mol a mol
XCO 3 → t ° XO + CO 2
2a mol 2a mol
Theo phương trình hoá học trên và dữ kiện đề bài, ta có :
Giải hệ phương trình trên ta thu được : X = 24 (Mg).