Hỗn hợp khí A chứa etilen và hidro có tỉ khối so với hidro là 7,5. Dẫn A qua xúc tác Ni nung nóng thu được hỗn hợp B có tỉ khối so với hidro là 12,5. Tính hiệu suất phản ứng cộng hidro của etilen.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


trong 1 mol hh ban đầu có nH2 =0,75 mol , nC2H4 =0,25 mol
nsau= 2,125.13/34=0,8125
=> nH2 pứ =ntrc -nsau =1- 0.8125=0,1875
=> H= 0,1875/0,75 .100= 25%

Đáp án B
Đáp án
Gọi a, b là số mol C2H4 và H2 trước phản ứng.
Ta có: 28 a + 2 b a + b = 4,25.2 = 8,5
<=> 28a + 2b = 8,5a + 8,5b <=> 19,5a = 6,5b => a = b 3 hay b = 3a
PTPU: C2H4 + H2 → N i , t 0 C2H6
Trước p/ư: a 3a
P/ư: 0,75a 0,75a
Sau p/ư: 0,25a 2,25a 0,75a
d Y H 2 = 0 , 25 . a . 28 + 2 , 25 . a . 2 + 0 , 75 . 3 a 3 , 25 a . 2
= 5,23

Đáp án A
Hướng dẫn : M - A = 2. 7,5 = 15
Giả sử nA = 1mol → mB = mA = 15. 1 = 15 g ; nC2H4 : nH2 = 1:1
Mà M - B = 9. 2 = 18 → nB = 0,83 mol → nH2 pư = 1 – 0,83 = 0,167 mol
→ H = 0 , 176 0 , 5 .100% = 33,3%

Coi n X = 1(mol)
Gọi n H2 = a(mol) ; n N2 = b(mol)
Ta có :
a + b = 1
2a + 28b = 3,6.2 = 7,2
=> a = 0,8 ; b = 0,2
3H2 + N2 \(\xrightarrow{t^o,xt}\)2 NH3
3a........a..............2a........(mol)
Vì n H2 / 3 > n N2 / 1 nên hiệu suất tinh theo số mol N2
Gọi hiệu suất là a => n N2 pư = a(mol)
m Y = m X = 7,2
=> n Y = 7,2/(4,2826.2) = 0,84(mol)
Sau phản ứng, Y gồm :
H2 : 0,8 - 3a
N2 : 0,2 - a
NH3 : 2a
=> n Y = 0,8 - 3a + 0,2 -a + 2a = 0,84
=> a = 0,08 = 8%

Đáp án C
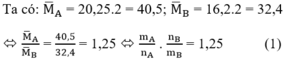
Áp dụng định luật bảo toàn khối lượng ta có: mA = mB
![]()
Giả sử ban đầu có 1 mol hỗn hợp A => nB = 1,25.1 = 1,25 mol
Trong phản ứng đề hidro hóa: số mol hỗn hợp khí sau phản ứng tăng, số mol tăng của hỗn hợp B so với hỗn hợp A chính là số mol các chất phản ứng.
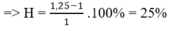

Đáp án : C
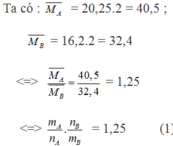
Áp dụng định luật bảo toàn khối lượng ta có: mA = mB
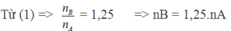
Giả sử ban đầu có 1 mol hỗn hợp A => nB = 1,25.1 = 1,25 mol
Trong phản ứng đề hidro hóa: số mol hỗn hợp sau phản ứng tăng, số mol tăng của hỗn hợp B so với hỗn hợp A chính là số mol các chất phản ứng
=> H = (1,25-1) .100% = 25%

Đây là một ví dụ rất đơn giản nhưng đặc trưng về quan hệ số mol trong phản ứng cộng hidro của hidrocacbon chưa no
Dễ tính đươc
![]()
Trong phản ứng hidro hóa hidrocacbon chưa no thì số mol khí giảm chính bằng số mol hidro phản ứng suy ra ![]()
Mặt khác đề cho hidrocacbon dư, phản ứng hoàn toàn nên
![]()
suy ra ![]()

Hoàn toàn tương tự bài toán trước. Có thể tự chọn lượng chất rồi bảo toàn khối lượng cho phản ứng, hoặc một cách nhanh hơn là áp dụng công thức:

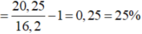
Vậy đáp án đúng là A
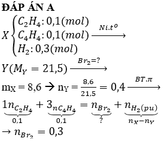
Vì khối lượng của hỗn hợp trước và sau phản ứng là bằng nhau
=> n hh trước phản ứng : n hh sau phản ứng = 25 : 15 = 5 : 3
Coi tổng số mol trước phản ứng là 5 => tổng số mol sau phản ứng là 3 mol
Ta có khối lượng hỗn hợp là : 5 . 15 = 75 g
Ta có hệ :
Ban đầu 2,5 2,5
Phản ứng x x
Kết thúc : 2,5 – x 2,5– x x
=> Tổng số mol sau phản ứng là : : 2,5 – x + 2,5– x + x = 5–x
=> 5 – x = 3 => x = 2 mol