cho 0,2 mol Fe phản ứng với 0,1 mol S . tính khối lượng của sản phẩm , tìm chất dư và khối lượng của chất dư
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


C9:
nP = 6,2/31 = 0,2 (mol)
nO2 = 6,4/32 = 0,2 (mol)
PTHH: 4P + 5O2 -> (t°) 2P2O5
LTL: 0,2/4 > 0,2/5 => P dư
nP (p/ư) = 0,2/5 . 4 = 0,16 (mol)
nP (dư) = 0,2 - 0,16 = 0,04 (mol)
nP2O5 = 0,2/5 . 2 = 0,08 (mol)
mP2O5 = 0,08 . 142 = 11,36 (g)
C10:
Áp dụng ĐLBTKL, ta có:
mR + mO2 = mRO
=> mO2 = 21,6 - 16,8 = 4,8 (g(
=> nO2 = 4,8/32 = 0,15 (mol)
PTHH: 2R + O2 -> (t°) 2RO
nR = 0,15 . 2 = 0,3 (mol)
M(R) = 16,8/0,3 = 56 (g/mol(
=> R là Fe

\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
Lập tỉ lệ :
\(\dfrac{0.3}{2}< \dfrac{0.2}{1}\)
\(\Rightarrow H_2SO_4dư\)
\(m_{Na_2SO_4}=0.15\cdot142=21.3\left(g\right)\)
\(m_{H_2SO_4\left(dư\right)}=\left(0.2-0.15\right)\cdot98=4.9\left(g\right)\)

Bài 1:
a) nP=6,2/31=0,2(mol); nO2= 6,72/22,4=0,3(mol)
PTHH: 4P + 5 O2 -to-> 2 P2O5
Ta có: 0,2/4 < 0,3/5
=> P hết, O2 dư, tính theo nP
=> nO2(p.ứ)= 5/4. nP= 5/4. 0,2=0,25(mol)
=> mO2(dư)=0,3- 0,25=0,05(mol)
=> mO2(dư)=0,05.32=1,6(g)
b) nP2O5= nP/2= 0,2/2=0,1(mol)
=>mP2O5=0,1.142=14,2(g)

Có lẽ đề cho nung kết tủa trong không khí chứ không phải "để" bạn nhỉ?
PT: \(Zn+CuSO_4\rightarrow ZnSO_4+Cu\)
____0,04_____0,04_____0,04 (mol)
\(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
0,03_____0,03______0,03 (mol)
⇒ nCuSO4 dư = 0,1 - 0,04 - 0,03 = 0,03 (mol)
- Dung dịch X gồm: ZnSO4: 0,04 (mol), FeSO4: 0,03 (mol) và CuSO4: 0,03 (mol)
PT: \(ZnSO_4+Ba\left(OH\right)_2\rightarrow Zn\left(OH\right)_{2\downarrow}+BaSO_{4\downarrow}\)
______0,04__________________0,04______0,04 (mol)
\(Zn\left(OH\right)_2+Ba\left(OH\right)_2\rightarrow BaZnO_2+2H_2O\)
\(FeSO_4+Ba\left(OH\right)_2\rightarrow Fe\left(OH\right)_{2\downarrow}+BaSO_{4\downarrow}\)
0,03____________________0,03______0,03 (mol)
\(CuSO_4+Ba\left(OH\right)_2\rightarrow Cu\left(OH\right)_{2\downarrow}+BaSO_{4\downarrow}\)
0,03____________________0,03_______0,03 (mol)
- Kết tủa thu được gồm: Fe(OH)2: 0,03 (mol), Cu(OH)2: 0,03 (mol) và BaSO4: 0,1 (mol)
PT: \(4Fe\left(OH\right)_2+O_2\underrightarrow{t^o}2Fe_2O_3+4H_2O\)
_________0,03_________0,015 (mol)
\(Cu\left(OH\right)_2\underrightarrow{t^o}CuO+H_2O\)
0,03_________0,03 (mol)
⇒ m = mFe2O3 + mCuO + mBaSO4 = 0,015.160 + 0,03.80 + 0,1.233 = 28,1 (g)

1. Zn + 2AgNO3 ---> Zn(NO3)2 + 2Ag
x mol 2x
=> 2x. 108 - 65x = 3,02 => x = 0,02 mol
Vậy: Zn + O --> ZnO
=> m = 0,02. 61 = 1,62g
2. 2Al + 3CuCl2 ---> 2AlCl3 + 3Cu
0,1 mol 0,15 0,15
Fe + CuCl2 ---> FeCl2 + Cu
0,05 0,05 mol 0,05
Vậy: m = 0,2. 64 - 0,1.27 - 0,05.56 = 7,3g
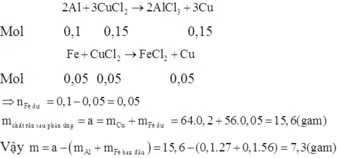

PTHH: \(Fe+S\xrightarrow[]{t^o}FeS\)
Xét tỉ lệ: \(\dfrac{0,2}{1}>\dfrac{0,1}{1}\) \(\Rightarrow\) Fe còn dư, tính theo S
\(\Rightarrow n_{FeS}=0,1\left(mol\right)=n_{Fe\left(dư\right)}\) \(\Rightarrow\left\{{}\begin{matrix}m_{FeS}=0,1\cdot88=8,8\left(g\right)\\m_{Fe\left(dư\right)}=0,1\cdot56=5,6\left(g\right)\end{matrix}\right.\)