Số oxi hóa của nguyên tố N trong các chất và ion N H 4 + , L i 3 N , H N O 2 , N O 2 , N O 3 - , K N O 3 lần lượt là
A. -3; -3; +3; +4; +5 và +5.
B. -3; -3; +3; +4; -5 và +5.
C. -3; +3; +3; +4; +5 và +5.
D. -4; -3; +3; +4; +5 và +5.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1.
- Al2O3: Số oxi hóa của O là -2.
Gọi a là số oxi hóa của Al. Áp dụng quy tắc 1 và 2
=> a.2 + (-2).3 = 0 → x = +3
Vậy số oxi hóa của O là -2, Al là +3
- CaF2
Gọi x là số oxi hóa của F, theo quy tắc 1 và 2 có:
1.(+2) + 2.x = 0 → x = -1.
Vậy số oxi hóa của Ca là +2, của F là -1.
2.
- N = O có công thức ion giả định là N2+O2-
Vậy số oxi hóa của N là +2, O là -2.
- CH4 có công thức ion giả định là C4-H4+
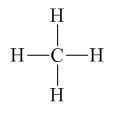
Vậy số oxi hóa của C là -4, H là +1.

Mik làm nhanh luôn nhé.
a. S(IV), S(VI), S(II)
b. N(II), N(III), N(I), N(V)
c. P(III), P(V)
d. Fe(II), Fe(III), Fe(II), Fe(III)
nguyên tố nito có số oxi hóa là bao nhiêu trong các hợp chất sau : NH3 , NH4Cl , N2O , N2O3 , N2O5 ?


1. \(CTTQ:RO_2\)
Theo đề bài ta có:
\(R+2.16=64\Leftrightarrow R=64-32=32\)
\(\rightarrow R:S \)
\(\rightarrow CTHH:SO_2\)
2. \(CTTQ:XO\)
Theo đề bài ta có:
\(\frac{X}{16}=\frac{80}{20}\Leftrightarrow X=64\)
\(\rightarrow X:Cu\)
\(\rightarrow CTHH:CuO\)
\(3.CTTQ:P_xO_y\)
Theo đề bài ta có:
\(\frac{31x}{16y}=\frac{31}{40}\Leftrightarrow\frac{x}{y}=\frac{2}{5}\Leftrightarrow\left\{{}\begin{matrix}x=2\\y=5\end{matrix}\right.\)
\(\rightarrow CTHH:P_2O_5\)
\(\rightarrow CTHH:SO_2\)
bài 1/
có: PTKRO2= NTKR+ 2.NTKO
\(\Rightarrow\) 64= NTKR+ 32
\(\Rightarrow\) NTKR= 32
vậy R là lưu huỳnh( S)
bài 2/
X hóa trị II\(\Rightarrow\) oxit của X: XO
có: \(\frac{16}{X+16}\)= 0,2
\(\Rightarrow\) X= 64
vậy X là đồng
KH: Cu
bài 3/
gọi CTTQ của chất đó là PaOb
a:b= \(\frac{31}{31}\): \(\frac{40}{16}\)
= 1: 2,5
= 2: 5
\(\Rightarrow\) a= 2
b= 5
\(\Rightarrow\) CTHH: P2O5

1, Gọi CTTQ của hợp chất là X2O3
Ta có: 2Mx + 3MO = 160
=> Mx = \(\dfrac{160-48}{2}\) = 56
=> X là Fe
Đáp án A
Số oxi hóa của các nguyên tố là: