Nguyên tử X có tổng số hạt proton, nơtron, electron là 115 và số khối là 80. Số lớp electron và số electron ở lớp ngoài cùng của X lần lượt là
A. 4 và 7
B. 3 và 5
C. 3 và 7
D. 4 và 1
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn B
Gọi số proton, nơtron và electron trong X lần lượt là p, n và e.
Theo bài ra ta có hệ phương trình:
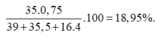
Cấu hình electron nguyên tử X là: [ A r ] 3 d 10 4 s 2 4 p 5 . Vậy X có 4 lớp electron và 7electron lớp ngoài cùng.

\(Tacó:\left\{{}\begin{matrix}2Z+N=60\\Z+N=40\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}Z=20\\N=20\end{matrix}\right.\\CHecủaX:1s^22s^2 2p^63s^23p^64s^2\\ \Rightarrow4lớpe,2engoàicùng\)

Ta có :
$2p + n = 18 \Rightarrow n = 18 -2 p$
Mặt khác:
$p ≤ n ≤ 1,5p$
$\Rightarrow p ≤ 18 - 2p ≤ 1,5p$
$\Rightarrow 5,14 ≤ p ≤ 6$
Với p = 6 thì thỏa mãn. Suy ra$ n = 6$
phân lớp ngoài cùng có 4 electron
Đáp án C

Gọi phân lớp ngoài cùng của 2 nguyên tử A, B lần lượt là 3pa và 4sb
Vì phân lớp 4s chỉ có tối đa 2 electron nên hiệu số của 2 phân lớp là hiệu số giữa phân lớp 3p của nguyên tử A với phân lớp 4s của nguyên tử B. (a<b)
Ta có hpt: \(\left\{{}\begin{matrix}a+b=5\\a-b=3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=4\\b=1\end{matrix}\right.\)
=> Nguyên tử A có cấu hình: 1s22s22p63s23p4 => Z(A)= 16
=> P(A)=E(A)=Z(A)=16
=> Nguyên tử A có số hạt mang điện là: 16+16=32(hạt)
Nguyên tử B có cấu hình: 1s22s22p63s23p64s1 =>Z(B)=19
=> P(B)=E(B)=Z(B)=19
=> Nguyên tử B có số hạt mang điện là: 19+19=38(hạt)
Chúc em học tốt!

Nguyên tử lưu huỳnh có 3 lớp electron và 6 eletron lớp ngoài cùng
+ Khác: với nguyên tử O chỉ có 2 lớp electron.
+ Giống: với nguyên tử O là có cùng 6e ở lớp ngoài cùng.

B
Gọi số proton, nơtron và electron của X là p, n và e (trong đó p = e)
Theo bài ra ta có hệ phương trình:
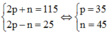
=> Cấu hình nguyên tử của X là
![]()
Chọn A
Số electron trong nguyên tử X là 115 – 80 = 35
Cấu hình electron trong nguyên tử của X là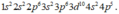 . Vậy X có 4 lớp electron và 7 electron lớp ngoài cùng.
. Vậy X có 4 lớp electron và 7 electron lớp ngoài cùng.