Đốt cháy một hiđrocacbon X bằng một lượng oxi vừa đủ. Sản phẩm tạo thành có tỉ khối so với hiđro là 133/9. Dẫn toàn bộ sản phẩm qua 50ml dung dịch KOH 1M (D = 1,0353 g/cm3) thì thấy khối lượng dung dịch tăng 2,66 gam. Vậy công thức phân tử của X là:
A. C3H6
B. C3H8
C. C4H10
D. C4H8

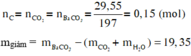
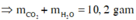
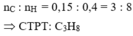
Sản phẩm gồm CO2 và H2O
Đặt nCO2 = a ; nH2O = b; Mhỗn hợp = 2.133/9 = 266/9
⇒ 44a + 18b = 266/9.(a+b) (1)
Dẫn toàn bộ sản phẩm qua 50ml dung dịch KOH 1M (D = 1,0353 g/cm3) thì thấy khối lượng dung dịch tăng 2,66 gam
⇒ mCO2 + mH2O = 2,66 ⇒ 44a + 18b = 2,66 (2)
Từ (1) và (2) ⇒ a= 0,04 ; b = 0,05
nCO2 : nH2O = 0,04 : 0,05
⇒ nC : nH = 4 : 10
⇒X là C4H10
Đáp án C.