Một dung dịch X có chứa a mol NH4+, b mol Ba2+ và c mol Cl-. Nhỏ dung dịch Na2SO4 đến dư vào dung dịch X thu được 34,95 gam kết tủa. Mối quan hệ giữa a và c là:
A. c - a = 0,3
B. a = c
C. a - c = 0,3
D. a + c = 0,3
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

n H + = 2 n H 2 S O 4 = 0 , 15 . 2 = 0 , 3 ; n S O 4 2 - = 0 , 15 v à n C O 3 2 - = 0 , 1 ; n H C O 3 - = 0 , 3
Xác định tỉ lệ số mol của C O 3 2 - v à H C O 3 - và trong dung dịch ta có:
n N a 2 C O 3 n N a H C O 3 = 0 , 1 0 , 3 = 1 3
So sánh số mol: Ta có: ( 2 n C O 3 2 - + n H C O 3 2 - ) = 0 , 5 > n H + = 0 , 3 ⇒ H + h ế t
Khi cho từ từ A vào B nên C O 3 2 - và H C O 3 - sẽ đồng thời phản ứng với axit.
Vì vậy giả sử nếu C O 3 2 - phản ứng hết x mol thì H C O 3 - sẽ phản ứng 1 lượng đúng bằng tỉ lệ mol trong dung dịch của 2 chất là 3x mol.
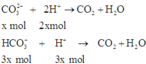
Do H+ hết nên tính theo H+ ta có: 5x = 0,3 ⇒ x = 0,6
⇒ Trong X chứa anion: H C O 3 - (0,3 – 3.0,6 = 0,12 mol), C O 3 2 - (0,1 – 0,06 = 0,04 mol) và S O 4 2 - (0,15 mol)
Khi cho Ba(OH)2 dư vào ta có các phản ứng:
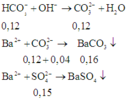
Vậy khối lượng kết tủa thu được là:
![]()

Chọn đáp án B
Bảo toàn điện tích: ∑nđiện tích (+) = ∑nđiện tích (-).
⇒ a + 3b + 2c = x + y ⇒ chọn B.

Theo định luật bảo toàn điện tích:
\(a+b=n_{Na^+}+2n_{Mg^{2+}}\Rightarrow a+b=0,4\) (1)
Để đơn giản, ta xét toàn bộ lượng dung dịch X tác dụng với dung dịch AgNO3 dư, ta có:
\(n_{AgCl}=\dfrac{2,1525.10}{143,5}=0,15\left(mol\right)\)
\(Ag^++Cl^-\rightarrow AgCl\downarrow\)
0,15 <-- 0,15
\(\Rightarrow a=n_{Cl^-}=0,15\left(mol\right)\Rightarrow b=0,4-0,15=0,25\left(mol\right)\)
Muối khan thu được khi cô cạn dung dịch X là:
\(m_{\text{muối}}=0,1.23+0,15.24+0,15.35,5+0,25.62=26,725\left(gam\right)\)
Theo định luật bảo toàn điện tích:
\(a+b=n_{Na^+}+2n_{Mg^{2+}}\Rightarrow a+b=0,4\) (1)
Để đơn giản, ta xét toàn bộ lượng dung dịch X tác dụng với dung dịch AgNO3 dư, ta có:
\(n_{AgCl}=\dfrac{2,1525.10}{143,5}=0,15\left(mol\right)\)
\(Ag^++Cl^-\rightarrow AgCl\downarrow\)
0,15 <-- 0,15
\(\Rightarrow a=n_{Cl^-}=0,15\left(mol\right)\Rightarrow b=0,4-0,15=0,25\left(mol\right)\)
Muối khan thu được khi cô cạn dung dịch X là:
\(m_{\text{muối}}=0,1.23+0,15.24+0,15.35,5+0,25.62=26,725\left(gam\right)\)

\(n_{NaOH}=\dfrac{200.10\%}{40}=0,5\left(mol\right)\)
\(PTHH:CuCl_2+2NaOH\rightarrow2NaCl+Cu\left(OH\right)_2\)
bđ: 0,3 0,5
pứ: 0,25 0,5 0,5 0,25
[ ]: 0,05 0 0,5 0,25
\(PTHH:Cu\left(OH\right)_2\underrightarrow{t^o}CuO+H_2O\)
(mol) 0,25 0,25
\(a.m_C=80.0,25=20\left(g\right)\)
\(b.m_{NaCl}=58,5.0,5=29,25\left(g\right)\\ m_{Cu\left(OH\right)_2}=0,25.98=24,5\left(g\right)\\ m_{CuCl_2\left(du\right)}=135.0,05=6,75\left(g\right)\)
\(c.m_{ddspu}=100+200-24,5=275,5\left(g\right)\\ C\%_{ddCuCl_2\left(du\right)}=\dfrac{135.0,05}{275,5}.100=2,45\left(\%\right)\\ C\%_{ddNaCl}=\dfrac{0,5.58,5}{275,25}.100=10,62\left(\%\right)\)
Đáp án A
Ba2++ SO42- → BaSO4
nSO4(2-) = nBaSO4 = 34,95/233=0,15 mol = nBa2+
Theo ĐLBT ĐT thì a+2b = c suy ra a+2.0,15 = c nên c-a = 0,3