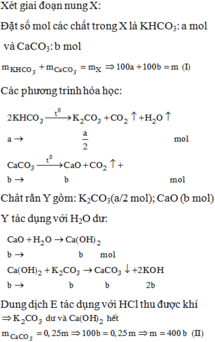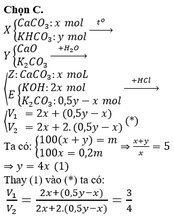Nung m gam hỗn hợp X gồm KHCO3 và CaCO3 ở nhiệt độ cao đến khi khối lượng không đổi thu được chất rắn Y. Cho Y vào nước dư, thu được 0,25m gam chất rắn Z và dung dịch E. Nếu nhỏ từ từ dung dịch HCl vào E, khi khí bắt đầu thoát ra cần dùng V1 lít dung dịch HCl 1M. Còn nếu nhỏ từ từ dung dịch HCl vào E, khí thoát ra hết thì thể tích dung dịch HCl 1M đã dùng là V2 lít. Tính thể tích V1:V2.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

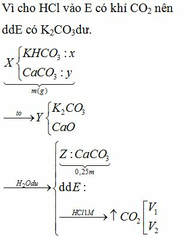
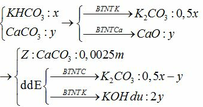
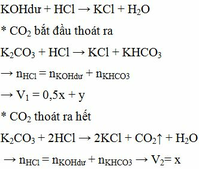
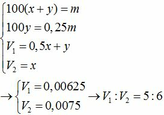

Do khi nhỏ HCl vào E thu được khí
=> Trong dd E chứa K2CO3
=> Ca2+ bị kết tủa hết
mZ = mCaCO3 = 0,25m (g)
=> \(n_{CaCO_3\left(Z\right)}=\dfrac{0,25m}{100}=0,0025m\left(mol\right)\)
Bảo toàn Ca: \(n_{CaCO_3\left(X\right)}=0,0025m\left(mol\right)\)
=> \(m_{KHCO_3}=m-100.0,0025m=0,75m\left(g\right)\)
=> \(n_{KHCO_3\left(X\right)}=\dfrac{0,75m}{100}=0,0075m\left(mol\right)\)
=> \(n_{K_2CO_3\left(Y\right)}=0,00375m\left(mol\right)\)
Bảo toàn C: \(n_{K_2CO_3\left(E\right)}=0,00375m-0,0025m=0,00125m\left(mol\right)\)
Bảo toàn K: \(n_{KOH}=2.0,00375m-2.0,00125m=0,005m\left(mol\right)\)
PTHH: KOH + HCl --> KCl + H2O
0,005m->0,005m
=> \(V_1=\dfrac{0,005m}{1}=0,005m\left(l\right)\)
K2CO3 + 2HCl --> 2KCl + CO2 + H2O
0,00125m->0,0025m
=> \(V_2=\dfrac{0,0025m+0,005m}{1}=0,0075m\left(l\right)\)
=> \(\dfrac{V_1}{V_2}=\dfrac{0,005m}{0,0075m}=\dfrac{2}{3}\)

Đáp án C
Giả sử m = 10 g, khi đó n(X) = 0,1 mol
Theo dữ kiện đề bài thì khi cho Y vào nước dư thu được 0,025 mol CaCO3
→ hỗn hợp X chứa 0,025 mol CaCO3 và 0,075 mol KHCO3. Các quá trình phản ứng xảy ra:
2KHCO3 → K2CO3 + CO2
CaCO3 → CaO + CO2
Khi cho Y vào nước dư thì:
K2CO3 + CaO + H2O → CaCO3 + 2KOH
Vậy dung dịch E gồm K2CO3 dư (0,0125) và KOH (0,05)
PT:
H+ + OH- → H2O
H+ + CO32- → HCO3-
H+ + HCO3- → CO2 + H2O
Lượng HCl cho vào E đến khi bắt đầu thoát khí là:
n(HCl)1 = n(K2CO3) + n(KOH) = 0,0625
Lượng HCl cho vào E đến khi thoát hết khí là:
n(HCl)2 = 2n(K2CO3) + n(KOH) = 0,075
=> n(HCl)1 : n(HCl)2 = 5:6

Đáp án C
Giả sử m = 10 g, khi đó n(X) = 0,1 mol
Theo dữ kiện đề bài thì khi cho Y vào nước dư thu được 0,025 mol CaCO3
→ hỗn hợp X chứa 0,025 mol CaCO3 và 0,075 mol KHCO3. Các quá trình phản ứng xảy ra:
2KHCO3 → K2CO3 + CO2
CaCO3 → CaO + CO2
Khi cho Y vào nước dư thì:
K2CO3 + CaO + H2O → CaCO3 + 2KOH
Vậy dung dịch E gồm K2CO3 dư (0,0125) và KOH (0,05)
PT:
H+ + OH- → H2O
H+ + CO32- → HCO3-
H+ + HCO3- → CO2 + H2O
Lượng HCl cho vào E đến khi bắt đầu thoát khí là:
n(HCl)1 = n(K2CO3) + n(KOH) = 0,0625
Lượng HCl cho vào E đến khi thoát hết khí là:
n(HCl)2 = 2n(K2CO3) + n(KOH) = 0,075
=> n(HCl)1 : n(HCl)2 = 5:6

Dung dịch E chứa $KOH$ và $K_2CO_3$
Bảo toàn C ta có: $n_{K_2CO_3/(pu)}=0,15(mol)$
Bảo toàn $H^+$ ta có: $n_{KOH/(pu)}=0,1(mol)$
Nhận thấy phản ứng tỉ lệ với nhau là $n_{K_2CO_3}:n_{KOH}=3:2$
Đặt: $n_{K_2CO_3/E}=3a;n_{KOH/E}=2a$
Bảo toàn $OH^-$ ta có: $n_{Ca(OH)_2}=n_{CaCO_3}=a(mol)$
Bảo toàn K ta có: $n_{KHCO_3}=8a(mol)$
$\Rightarrow a=0,1\Rightarrow m=m_{CaCO_3}=10(g)$