Cho m gam hỗn hợp Fe và Zn tác dụng vừa hết với 1 lít dung dịch HCl 2,5M (D = 1,19 g/ml) thấy thoát ra một chất khí và thu được 1200 gam dung dịch. Xác định giá trị của m.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


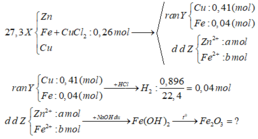
Các phản ứng xảy ra hoàn toàn, rắn Y + HCl giải phóng khí H2 => rắn Y gồm Cu và Fe dư
BT e : nFe dư = nH2 = 0,04 (mol)

Đáp án C

$Mg + 2HCl \to MgCl_2 + H_2$
$Zn + 2HCl \to ZnCl_2 + H_2$
$n_{H_2} = \dfrac{2,912}{22,4} = 0,13(mol)$
$n_{HCl} = 2n_{H_2} = 0,13.2 = 0,26(mol)$
Bảo toàn khối lượng :
$m = m_{muối} + m_{H_2} - m_{HCl} = 14,4 + 0,13.2 - 0,26.36,5 = 5,17(gam)$

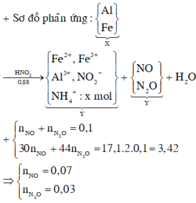
Đ á p á n B A l F e → 0 , 88 H N O 3 F e 2 + , F e 3 + A l 3 + , N O 3 - N H 4 + , x m o l N O N 2 O + H 2 O n N O + n N 2 O = 0 , 1 3 n N O + 44 n N 2 O = 17 , 1 . 2 . 0 , 1 = 3 , 42 ⇒ n N O = 0 , 07 n N 2 O = 0 , 03 B T N T H : n H 2 O = 0 , 88 - 4 x 2 = 0 , 44 - 2 x B T N T N : n N O 3 - ( Y ) = 0 , 81 - 0 , 3 . 2 - x = 0 , 75 - x B T N T H : 3 . 0 , 88 = 3 0 , 75 - x + 0 , 03 + 0 , 07 + 0 , 44 - 2 x m A l , F e = m m u ố i + m k h í + m H 2 O - m H N O 3 ⇒ x = 0 , 03 m A l , F e = 8 , 22 Y + d d N H 3 → k ế t t ủ a n O H - = 3 n A l 3 + + 3 n F e 3 + + 2 n F e 2 + = 0 , 75 - 0 , 03 - 0 , 03 = 0 , 69 m K T = m K L + m O H - = 8 , 22 + 0 , 69 . 17 = 19 , 95

Đáp án : C
P1 : nH2 = nFe = 0,1 mol
P2 : Gọi số mol của Fe và Cu trong P2 lần lượt là x và y
=> bảo toàn e : 3x + 2y = 2nSO2 = 0,8 mol
, mmuối = mCuSO4 + mFe2(SO4)3 = 200x + 160y = 56g
=> x = 0,2 ; y = 0,1 mol
Tỉ lệ mol Fe : Cu trong các phần không đổi
=>Trong P1 : nCu = 0,05 mol
Trong m gam X có: 0,3 mol Fe và 0,15 mol Cu
=> m = 26,4g
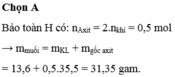


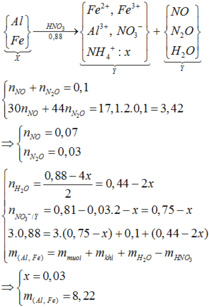
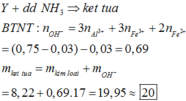

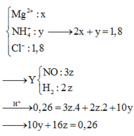
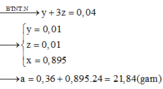
m dd HCl = 1000.1,19 = 1190 g
Áp dụng định luật bảo toàn khối lượng ta có:
m hh + 1190 = 1200 + m H 2
Phương trình hóa học của phản ứng:
Zn + 2HCl → Zn Cl 2 + H 2
Fe + 2HCl → Fe Cl 2 + H 2
Qua phương trình hóa học trên, ta nhận thấy:
n H 2 = 1/2 n HCl ; n H 2 = 2,5/2 = 1,25 mol
m hh = 1200 - 1190 +(1,25x2) = 12,5g