Cho 0,25 mol M n O 2 tác dụng với lượng dư HCl đặc, đun nóng. Thể tích khí clo thu được ở đktc là?
A. 2,24 lít.
B. 3,36 lít.
C. 5,6 lít.
D. 6,72 lít.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

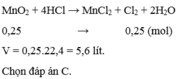

\(n_{MgCO_3}=\dfrac{12,6}{84}=0,15\left(mol\right)\)
\(MgCO_3+2HCl\rightarrow MgCl_2+H_2O+CO_2\)
0,15 0,15
\(V_{CO_2}=0,15.22,4=3,36\left(l\right)\)
--> A

Câu 24:
\(V_{H_2}=0,125.22,4=2,8\left(l\right)\)
→ Đáp án: D
Câu 25:
\(n_{CuO}=\dfrac{40}{80}=0,5\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Theo PT: \(n_{H_2}=n_{CuO}=0,5\left(mol\right)\) \(\Rightarrow V_{H_2}=0,5.22,4=11,2\left(l\right)\)
→ Đáp án: B
Câu 26:
\(m_{ZnO}=0,5.81=40,5\left(g\right)\)
→ Đáp án: A
Câu 27: B
Câu 28: B

2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2 + 6H2O
\(n_{SO_2}=\dfrac{3}{2}n_{Fe}=0,15\left(mol\right)\)
=> VSO2=0,15.22,4=3,36(lit)
=> Chọn C
Số mol của sắt
nFe = \(\dfrac{m_{Fe}}{M_{Fe}}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
Pt : Fe + 2H2SO4 → FeSO4 + SO2 + 2H2O\(|\)
1 2 1 1 2
0,1 0,1
Số mol của khí lưu huỳnh đioxit
nSO2 = \(\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
Thể tích của khí lưu huỳnh ddioxxit ở dktc
VSO2 = nSO2 . 22,4
= 0,1. 22,4
= 2,24 (l)
⇒ Chọn câu : A
Chúc bạn học tốt

1. B
2. B
(Câu 2 cậu nên sửa lại câu hỏi nhé: Khối lượng dung dịch NaOH 10% ...)
Câu 1.
\(n_{Fe}=\dfrac{5,6}{56}=0,1mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,1 0,1
\(V_{H_2}=0,1\cdot22,4=2,24\left(l\right)\)
Chọn B.
Câu 2. \(n_{HCl}=0,2\cdot1=0,2mol\)
Để trung hòa: \(\Rightarrow n_{H^+}=n_{OH^-}=0,2\)
\(m_{NaOH}=0,2\cdot40=8\left(g\right)\)
\(m_{ddNaOH}=\dfrac{8}{10\%}\cdot100\%=80\left(g\right)\)
Chọn B.