1. Cho 9.2g khối lượng A hóa trị 2 phản ứng với cl dư tạo thành 23,4g muối .Xđ tên kim loại A
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


1. \(2A+Cl_2\rightarrow2ACl\)
\(m_{2A}=9,2g;m_{ACl}=m_{A+35,5}=23,4g\)
Ta có tỉ lệ: \(\dfrac{2A}{9,2}=\dfrac{2\left(A+35,5\right)}{23,4}\)
\(\Rightarrow46,8A=18,4A+653,2\)
\(\Rightarrow28,4A=653,2\)
\(\Rightarrow A=23\)
Vậy A là \(Na\)

Tham khảo:
Gọi nguyên tử khối của kim loại A là A.
Phương trình hóa học của phản ứng:
2A + Cl2 → 2ACl
mA = 9,2g, mACl = 23,4g.
Có nA = nACl
⇒ 9,2 x (A + 35,5) = A x 23,4.
⇒ A = 23. Vậy kim loại A là Na.
Hóa thì ít tham khảo lại nha cậu, nếu chưa học thì đừng làm =))

bảo toàn khối lượng ta có
mCl2= 23,4-9,2= 14,2g
nCl2=14,2/71=0,2mol
2A+Cl2-> 2ACl
0,4 0,2
M(A)= 9,2/0,4=23 (Na)
PTHH:2A+Cl2→2ACl
\(m_{Cl_2}=23,4-9,2=14,2\left(g\right)\)
\(n_{Cl_2}=\dfrac{14,2}{71}=0,2\left(mol\right)\)
⇒nA=0,2.2=0,4 (mol)
\(M_A=\dfrac{9,2}{0,4}=23\left(g/mol\right)\)
Vậy A là Natri

nH2 = 0,336/22,4 = 0,015 (mol)
PTHH: 2A + 6HCl -> 2ACl3 + 3H2
nACl3 = nA = 0,015 : 3 . 2 = 0,01 (mol)
M(A) = 0,27/0,01 = 27 (g/mol)
=> A là Al
mAlCl3 = 0,01 . 133,5 = 1,335 (g)
Câu 6.
\(n_{H_2}=\dfrac{0,336}{22,4}=0,015mol\)
\(2A+6HCl\rightarrow2ACl_3+3H_2\)
0,01 0,015
\(\overline{M_A}=\dfrac{0,27}{0,01}=27đvC\)
\(\Rightarrow A\) là Al nhôm.
\(m_{AlCl_3}=0,01\cdot133,5=1,335g\)
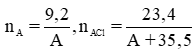
Đặt khối lượng là R
PTHH: \(2R+nCl_2\rightarrow^{t^o}2RCl_n\)
Theo phương trình \(n_R=n_{RCl_n}\)
\(\rightarrow\frac{9,2}{M_R}=\frac{23,4}{M_R+35,5n}\)
\(\rightarrow M_R=23n\)
Biện luận: Nếu \(n=1\rightarrow M_R=23\)
Vậy R là Na.