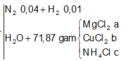
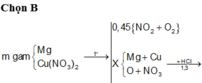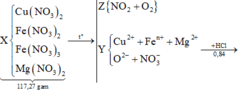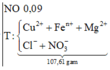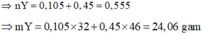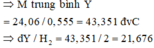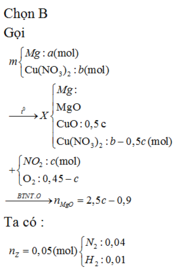Nung 0,12 mol hỗn hợp X gồm Fe(NO3)2, Cu(NO3)2, Zn(NO3)2 và m gam Al, trong một bình đựng chân không. Sau một thời gian thu được hỗn hợp rắn Y và 3,36 lít hỗn hợp khí Z(dktc). Hòa tan Y trong HCl loãng dư thì thấy có 0,62 mol HCl phản ứng, thu được dung dịch chứa 4 muối và V lít (dktc) một khí hóa nâu trong không khí. Tìm V
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Gọi số mol CO2, NO2, NH4+ và Al lần lượt là x, y, z, t.
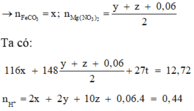
Dung dịch thu được khi cho Z tác dụng với NaOH chứa K+ 0,44 mol, SO42- 0,44 mol, AlO2- t mol.
Bảo toàn điện tích số mol Na+ là t+0,44
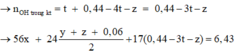
Giải được: x = 0,04; y = 0,01, z = 0,01; t = 0,08.
Số mol CO2 thu được khi nung X là 0,02 mol (BT C)
→ a = y + 0 , 02 = 0 , 03

Trong trường hợp này, X đã “bão hòa”, không thể cho e được nữa, nhưng nó đã được CO lấy đi một lượng O để phá vỡ trạng thái này. CO + [O] →CO2
Và thế là X trở thành Y, lại có thể cho e với N+5 tạo thành NO, NO2.
Theo lý thuyết, nếu HNO3 lại đưa Y lên trạng thái bão hòa thì số mol e mà N+5 nhận được là 0,24 x 2 = 0,48 mol
Nhưng trên thực tế, con số này là 0,11 x 3 + 0,07 x 1= 0,40 mol
Sở dĩ điều này xảy ra là do có một lượng Fe chỉ tồn tại ở số oxi hóa +2
→ nFe2+ = 0,48 – 0,40 =0,08 → mFe(NO3)2 = 14,4 gam
Chọn đáp án C

Ø Xét giai đoạn X tác dụng với dung dịch HCl:
![]()
![]() (NO là khí hóa nâu)
(NO là khí hóa nâu)
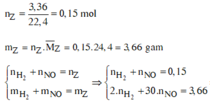
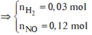
Thu được H2 => N O 3 - hết
Sơ đồ phản ứng:
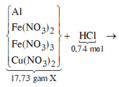
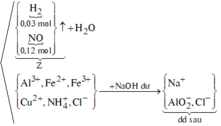
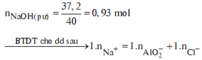
![]()
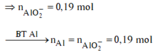
Các quá trình tham gia của H+:
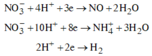
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Ø Xét giai đoạn X cho vào H2O dư:
Al là kim loại mạnh hơn Fe và Cu.
![]()
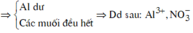
![]()
![]()
Sơ đồ phản ứng: 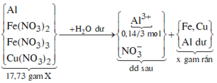
![]()
![]()
![]()
Đáp án C

Đáp án B

Từ (1), (2), (3), (4), (5) suy ra
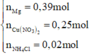
=> m=24.0,39+188.0,25=56,36 gam gần với giá trị 55 nhất.