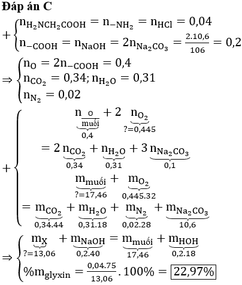
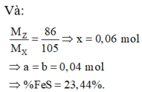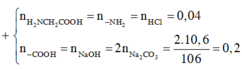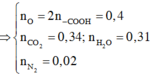Hỗn hợp X gồm FeS2 và Cu2S có khối lượng m1 gam. Đốt cháy hết m1 gam X bằng khí oxi,
thu được hỗn hợp rắn Y gồm hai oxit có khối lượng 8 gam. Chia Y thành hai phần bằng nhau.
- Phần 1: Tác dụng vừa hết với 2,8 lít H2 (đktc).
- Phần 2: Tác dụng vừa hết với m2 gam dung dịch H2SO4 24,5%.
a) Tính các giá trị m1 và m2.
b) Tính thể tích khí oxi (đktc) cần để đốt cháy hết m1 gam X.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Phần 1:
Gọi: \(\left\{{}\begin{matrix}n_{Mg}=x\left(mol\right)\\n_{Al}=y\left(mol\right)\\n_{Cu}=z\left(mol\right)\end{matrix}\right.\) (trong phần 1)
⇒ 24x + 27y + 64z = 3,48 (1)
PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Theo PT: \(n_{HCl}=2n_{Mg}+3n_{Al}=2x+3y=0,16\left(2\right)\)
- Phần 2:
Mg, Al, Cu có số mol lần lượt là: kx, ky, kz (mol)
PT: \(2Mg+O_2\underrightarrow{t^o}2MgO\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(2Cu+O_2\underrightarrow{t^o}2CuO\)
Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{Mg}+\dfrac{3}{4}n_{Al}+\dfrac{1}{2}n_{Cu}=\dfrac{1}{2}kx+\dfrac{3}{4}ky+\dfrac{1}{2}kz=0,165\left(3\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Theo PT: \(n_{H_2}=n_{CuO}=n_{Cu}=kz=0,09\left(4\right)\)
Từ (3) và (4) có: \(\dfrac{kz}{\dfrac{1}{2}kx+\dfrac{3}{4}ky+\dfrac{1}{2}kz}=\dfrac{0,09}{0,165}\Rightarrow\dfrac{z}{\dfrac{1}{2}x+\dfrac{3}{4}y+\dfrac{1}{2}z}=\dfrac{6}{11}\)
⇒ 3x + 4,5y - 8z = 0 (5)
Từ (1), (2) và (5) \(\Rightarrow\left\{{}\begin{matrix}x=0,02\left(mol\right)\\y=0,04\left(mol\right)\\z=0,03\left(mol\right)\end{matrix}\right.\)
Thay vào (4) ⇒ k = 3
Vậy: nMg = x + kx = 0,08 (mol) ⇒ mMg = 0,08.24 = 1,92 (g)
nAl = y + ky = 0,16 (mol) ⇒ mAl = 0,16.27 = 4,32 (g)
nCu = z + kz = 0,12 (mol) ⇒ mCu = 0,12.64 = 7,68 (g)