Cho 16 g oxit sắt tác dung vừa đủ với 120 ml dd HCl . Sau phản ứng thu được 32,5 g muối khan. Tìm CTPT oxit sắt.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Hơi làm biếng viết chỉ số cho rõ nên chịu khó coi giùm mk
Gọi CT oxit sắt: FexOy
FexOy + 2yHCl => xFeCl2y/x + yH2O
Theo đề bài, ta có:
\(\frac{32x}{56x+16y}=\frac{65}{56+71\frac{y}{x}}\)
1792x + 2272y = 3640x + 1040y
1848x = 1232y => x/y = 2/3
CT: Fe2O3

Fe x O y + 2yHCl → x FeCl 2 y / x + y H 2 O
Theo phương trình : (56x + 16y) gam cho (56x + 71y) gam muối
Theo đề bài: 7,2 gam cho 12,7 gam
Giải ra, ta có : x/y = 1/1 . Công thức oxit săt là FeO.

Tương tự bài 1 và bài 4, ta có:
m 3 o x i t + m H C l = m m u o i + m H 2 O s a n p h a m
⇔ m 3 o x i t = m m u o i + m H 2 O s a n p h a m - m H C l
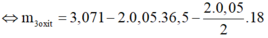
⇔ m 3 o x i t = 0,321g
⇒ Chọn D.

Giả sử công thức phân tử của oxit sắt là FexOy , phương trình phản ứng :
FexOy + 2yHCl \(\rightarrow\)xFeCl2y/x + yH2O
(56x+16y)g---------(56x+71y)g
7,2g-------------------12,7g
Theo phương trình phản ứng , ta có :
7,2(56x+71y) = 12,7(56x+16y)
\(\Leftrightarrow\)308x = 308y \(\Leftrightarrow\dfrac{x}{y}=\dfrac{1}{1}\)
Công thức oxit sắt là FeO
CTHH dạng TQ của oxit sắt là FexOy
PTHH :
FexOy + 2yHCl \(\rightarrow\) xFeCl2y/x + yH2O
- Vì t/d với HCl dư => oxit sắt hết
Đặt nHCl(Pứ) = a(mol) => mHCl(pứ) = 36,5a(g)
Theo PT => nH2O = 1/2 . nHCl = 1/2 .a(mol)
=> mH2O = 1/2 . a . 18 =9a(g)
Theo ĐLBTKL:
mFexOy + mHCl(pứ) = mmuối + mH2O
=> 7,2 + 36,5a = 12,7 + 9a
=>a = 0,2(mol)
=> nH2O = 1/2 . a = 1/2 . 0,2 = 0,1(mol)
=> nO / H2O = 0,1(mol)
=> mO / H2O = 0,1 . 16 = 1,6(g)
Theo ĐLBTKL :
mO / FexOy = mO / H2O = 1,6(g)
=> mFe / FexOy = mFexOy - mO / FexOy = 7,2 - 1,6 = 5,6(g)
=> nFe/FexOy = 5,6/56 = 01,(mol)
Ta Có :
x : y = nFe / FexOy : nO / FexOy = 0,1 : 0,1 = 1 : 1
=> x = y =1
=> CTHH của oxit sắt là FeO

PTHH:
\(CuO+2HCl->CuCl_2+H_2O\)
x.....................................x
\(Al_2O_3+6HCl->2AlCl_3\downarrow+3H_2O\)
y.........................................2y
Gọi x, y lần lượt là số mol của CuO, \(Al_2O_3\)
Ta có hệ PT: \(\left\{{}\begin{matrix}80x+102y=9,1\\135x+267y=20,1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,05\\y=0,05\end{matrix}\right.\)
=> \(m_{CuO}=0,05.80=4\left(g\right)\)
=> \(\%m_{CuO}=\dfrac{4}{9,1}.100\%=43,96\%\)
=> \(\%m_{Al_2O_3}=100\%-43,96\%=56,04\%\)
