X là hỗn hợp bột kim loại Cu và Fe, trong đó Fe chiếm 40% khối lượng. Hoà tan m gam X bằng 200 ml dung dịch \(HNO_3\) 2M thu được khí NO duy nhất, dung dịch Y và còn lại 0.7m gam kim loại. Khối lượng muối khan trong dung dịch Y là?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án : C
Vì mFe = 0,4m (g) . Mà Sau phản ứng còn 0,7m gam kim loại => có 0,3m gam kim loại phản ứng < 0,4m
=> Fe dư và phản ứng chỉ tạo Fe2+
3Fe + 8H+ + 2NO3- -> 3Fe2+ + 2NO + 4H2O
=> nFe2+ = 3/8.nHNO3 = 0,15 mol
=> mmuối = mFe(NO3)2 = 27g

Chất rắn không tan là Cu chưa pư.
⇒ mCu (dư) = 6 (g)
Ta có: 56nFe + 64nCu (pư) = 30 - 6 (1)
\(n_{HNO_3}=0,52.2=1,04\left(g\right)\Rightarrow n_{NO}=\dfrac{1,04}{4}=0,26\left(mol\right)\)
BT e, có: 2nFe + 2nCu (pư) = 3nNO = 0,78(2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Fe}=0,12\left(mol\right)\\n_{Cu\left(pư\right)}=0,27\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\%m_{Cu}=\dfrac{0,27.64+6}{30}.100\%=77,6\%\)

Đáp án : B
Hỗn hợp đầu + 0,4 mol HNO3 tạo khí NO hóa nâu trong không khí
Thêm 0,06666 mol H2SO4 hòa tan đủ kim loại thu được khí NO
=> Xét cả quá trình thì H+ phản ứng vừa hết với 12g kim loại ban đầu
=> nFe + nCu = 3 8 . n H + = 0,2 mol
Lại có : 56nFe + 64nCu = 12g
=> nFe = 0,1 mol
=> mFe = 5,6g

Chọn A
Theo bài ra cứ m gam X chứa 0,4m (gam) Fe và 0,6m (gam) Cu.
Vì chất rắn phản ứng nặng 0,65m (gam) > m C u nên Fe mới phản ứng một phần, dung dịch X chỉ có F e ( N O 3 ) 2
Gọi số mol Fe phản ứng là x (mol).
Bảo toàn electron: 2 . n F e = 3 . n k h i → n F e = 0,03 (mol)
Bảo toàn Fe có n m u ố i = m F e = 0,03.180 = 5,4 gam.

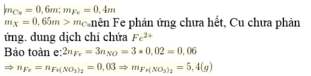

\(\left\{{}\begin{matrix}m_{Fe}=0,4m\left(g\right)\\m_{Cu}=0,6m\left(g\right)\end{matrix}\right.\)
Do sau phản ứng, KL dư => HNO3 thiếu
\(m_{KL}\) sau pư = 0,7m \(m_{Cu\left(bđ\right)}=0,6m\) => Fe dư
=> Sau pư có \(Fe^{+2}\), Fe dư và Cu k pư
Gọi số mol Fe phản ứng là a (mol)
\(n_{HNO_3}=0,2.2=0,4\left(mol\right)\)
Có: \(Fe^0-2e\rightarrow Fe^{+2}\)
____a----->2a----->a____(mol)
\(NO_3^-+4H^++3e\rightarrow NO+2H_2O\)
_______0,4 ----->0,3______________(mol)
Áp dụng ĐLBT e => 2a = 0,3
=> a = 0,15 (mol)
\(n_{Fe\left(NO_3\right)_2}=0,15\left(mol\right)\)
=> \(m_{Fe\left(NO_3\right)_2}=0,15.180=27\left(g\right)\)
giúp em bài này với ạ miyano shiho