Cho dung dịch chứa 3,25 gam hỗn hợp gồm NaBr và CaCl2 tác dụng với 108 ml dung dịch AgNO3 0,5 M. Sau khi bỏ kết tủa, người ta thêm HCl dư vào dung dịch thu được thì lại có thêm 0,574 gam kết tủa nữa. Tìm khối lượng của mỗi muối trong hỗn hợp ban đầu.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


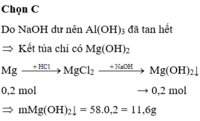
Do NaOH dư nên Al(OH)3 đã tan hết ⇒ Kết tủa chỉ có Mg(OH)2
Mg → + HCl MgCl2 → + NaOH Mg(OH)2↓
0,2 mol → 0,2 mol
⇒ mMg(OH)2↓ = 58.0,2 = 11,6g ⇒ Chọn C.

Đáp án : D
pH = 1 => CHCl = 0,1M => nHCl =0,04 mol
=> chất tan có : m = mAlCl3 + mFeCl2 + mHCl = 43,4
=> 133,5nAl + 127nFe = 41,94
Lại có 27nAl + 56nFe = 12,12
=> nAl = 0,2 ; nFe= 0,12 mol
=> nAg = 3nAl + 3nFe = 0,96 mol
=> mAg = 103,68g

Đáp án B.
CH3CHO -> 2Ag
C2H2 -> Ag2C2
Gọi số mol CH3CHO và C2H2 lần lượt là x và y
=> mhh = 44x + 26y = 8,04
Và mkết tủa = 216x + 240y = 55,2g
=> x = 0,1 ; y = 0,14 mol
Khi phản ứng với HCl chỉ có Ag2C2
Ag2C2 + 2HCl -> 2AgCl + C2H2
=> mkhông tan = mAgCl + mAg = 61,78g

Giải thích: Đáp án D
CH3CHO→2Ag
C2H2→Ag2C2
Gọi số mol CH3CHO và C2H2 lần lượt là x, y
→ mhh=44x+26y=8,04
m↓=216x+240y=55,2(g)
→ x = 0,2 và y = 0,14
Khi phản ứng với HCl chỉ có Ag2C2
→ khối lượng không tan= mAgCl+mAg=61,78 (g)

Đáp án D
CH3CHO→2Ag
C2H2→Ag2C2
Gọi số mol CH3CHO và C2H2 lần lượt là x, y
→ mhh=44x+26y=8,04
m↓=216x+240y=55,2(g)
→ x = 0,2 và y = 0,14
Khi phản ứng với HCl chỉ có Ag2C2
→ khối lượng không tan= mAgCl+mAg=61,78 (g)