Cho 1 luồng khí CO dư đi qua ống sứ chứa 24 g hỗn hợp gồm Fe2O3 và CuO nung nóng thu được hỗn hợp chất rắn Y có khối lượng 18,88 gam.Biết trong điều kiện thí nghiệm hiệu suất các phản ứng đều đạt 80%.Tính % về khối lượng của mỗi oxit trong hỗn hợp ban đầu .
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi \(\left\{{}\begin{matrix}n_{Fe2O3}:x\left(mol\right)\\n_{CuO}:y\left(mol\right)\end{matrix}\right.\)
\(Fe_2O_3+3CO\rightarrow2Fe+3CO_2\)
\(CuO+CO\rightarrow Cu+CO_2\)
\(160x+80y=24\)
\(n_{O\left(bi.khu\right)}=3n_{Fe2O3\left(pư\right)}+n_{CuO\left(pư\right)}=3x.80\%+y.80\%=\frac{24-18,88}{16}=0,32\left(mol\right)\)
\(\Rightarrow x=y=0,1\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe2O3}=\frac{160x}{24}=66,67\%\\\%m_{CuO}=100\%-66,67\%=33,33\%\end{matrix}\right.\)

\(n_{FeO}=a\left(mol\right),n_{ZnO}=b\left(mol\right)\)
\(m_{hh}=72a+81b=15.3\left(g\right)\left(1\right)\)
\(TC:n_{FeO\left(pư\right)}=0.8a\left(mol\right),n_{ZnO\left(pư\right)}=0.8b\left(mol\right)\)
\(FeO+CO\underrightarrow{t^0}Fe+CO_2\)
\(ZnO+CO\underrightarrow{t^0}Zn+CO_2\)
\(BTKL:\)
\(15.3+28n_{CO}=12.74+44n_{CO}\)
\(\Rightarrow n_{CO}=\dfrac{15.3-12.74}{44-28}=0.16\left(mol\right)\)
\(\Rightarrow0.8a+0.8b=0.16\left(2\right)\)
\(\left(1\right),\left(2\right):a=b=0.1\)
\(\%FeO=\dfrac{0.1\cdot72}{15.3}\cdot100\%=47.06\%\)
\(\%ZnO=52.94\%\)

bạn tự gọi ẩn nha :))))
PTFƯ: CO + FeO ==> Fe + CO2
.................a.........a..............a........a
CO + ZnO ===> Zn + CO2
................b..........b...............b...........b
nhìn vào phương trình phản ứng, ta có:
mhỗn hợp = mFeO + mZnO = 72a+ 81b = 15.5 (g)
mchất rắn thu đc nếu phản ứng hết = mthực tế : H= 9.68 : 80%=12.1
==> mFe + mZn = 56a + 65b = 12.1
Ta có hệ: 72a + 81b=15.5 và 56a + 65b = 12.1
== > a=0.19, b=0.022
==> %mFeO trong hh lúc đầu = \(\dfrac{0.19x72}{15.5}\) . 100% = 88.258%
===> %mZnO
bạn nhớ tick đúng cho mik nha ^_~
ọi x,y lần lượt là số mol của FeO và ZnO trong hỗn hợp.
=> 72x + 81y = 15,3 gam (1)
FeO + CO --> Fe + CO2
ZnO + CO --> Zn + CO2
** Cách 1:
H = 80% => Hỗn hợp chất rắn sau phản ứng gồm: 0,8x mol Fe, 0,8y mol Zn, 0,2x mol FeO và 0,2y mol ZnO
Ta có PT: 0,8x.56 + 0,8y.65 + 0,2x.72 + 0,2x.81 = 12,74 <=> 59,2x + 68,2y = 12,74 (2)
(1) và (2) => x = y = 0,1 mol => %FeO = 47,06%; %ZnO = 52,94%
*** Cách 2:
Số mol FeO và ZnO đã phản ứng là 0,8x mol và 0,8y mol.
Áp dụng định luật bảo toàn khối lượng:
15,3 + mCO = 12,74 + mCO2 => 2,56 = 0,8(x+y).44 - 0,8(x+y).28 => 12,8(x+y) = 2,56
<=> x + y = 0,2 (3)
Từ (1) và (3) => x = y = 0,1 mol

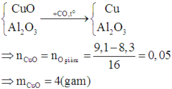
Đáp án:
→%mFe2O3=66,67%;%mCuO=33,33%→%mFe2O3=66,67%;%mCuO=33,33%
Giải thích các bước giải:
Gọi số mol 2 oxit lần lượt là x, y.
→160x+80y=24 gam→160x+80y=24 gam
Phản ứng xảy ra:
Fe2O3+3CO→2Fe+3CO2Fe2O3+3CO→2Fe+3CO2
CuO+COto→Cu+CO2CuO+CO→toCu+CO2
Khối lượng rắn giảm là do O bị khử
→nO bị khử=3nFe2O3 phản ứng+nCuO phản ứng=3x.80%+y.80%=24−18,8816=0,32 mol→nO bị khử=3nFe2O3 phản ứng+nCuO phản ứng=3x.80%+y.80%=24−18,8816=0,32 mol
Giải được: x=y=0,1.
→%mFe2O3=160x24=66,67%→%mCuO=33,33%