Hai lá sắt có khối lượng bằng nhau và bằng 11,2 g. Một lá cho tác dụng hết với khí clo, một lá ngâm trong dung dịch HCl dư. tính khối lượng muối tạo ra trong 2 th
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(Fe+CuSO_4\to FeSO_4+Cu\)
Đặt \(n_{CuSO_4}=x(mol)\)
\(\Rightarrow 64x-56x=2\\ \Rightarrow x=0,25(mol)\\ \Rightarrow n_{Fe}=n_{Cu}=0,25(mol)\\ \Rightarrow m_{Fe}=0,25.56=14(g);m_{Cu}=0,25.64=16(g)\)

Bài 1:
\(PTHH:Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag\\ \Rightarrow n_{Ag}=2n_{Cu}\\ m_{tăng}=m_{Ag}-m_{Cu}=15,2\left(g\right)\\ \Rightarrow108n_{Ag}-64n_{Cu}=15,2\\ \Rightarrow216n_{Cu}-64n_{Cu}=15,2\\ \Rightarrow n_{Cu}=0,1\left(mol\right)\\ \Rightarrow n_{AgNO_3}=0,2\left(mol\right)\\ \Rightarrow C_{M_{AgNO_3}}=\dfrac{0,2}{0,5}=0,4M\)
Bài 2:
\(n_A=\dfrac{78}{M_A}\left(mol\right);n_{ACl}=\dfrac{149}{M_A+35,5}\left(mol\right)\\ PTHH:2A+Cl_2\rightarrow2ACl\\ \Rightarrow n_A=n_{ACl}\Rightarrow\dfrac{78}{M_A}=\dfrac{149}{M_A+35,5}\\ \Rightarrow78M_A+2769=149M_A\\ \Rightarrow71M_A=2769\\ \Rightarrow M_A=39\\ \Rightarrow A\text{ là kali }\left(K\right)\)
Bài 3:
\(a,2Al+3ZnSO_4\rightarrow Al_2\left(SO_4\right)_3+3Zn\\ b,Mg+H_2SO_4\rightarrow MgSO_4+H_2\\ MgO+H_2SO_4\rightarrow MgSO_4+H_2O\\ MgCO_3+H_2SO_4\rightarrow MgSO_4+H_2O+CO_2\uparrow\)

Bài 1 :
Pt : \(Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag|\)
1 2 1 2
x 0,2 2x
Gọi x là số mol của Cu
Vì khối lượng của đồng tăng so với ban đầu nên ta có phương trình :
\(m_{Ag}-m_{Cu}=15,2\left(g\right)\)
\(108.2x-64.x=15,2\)
\(216x-64x=15,2\)
\(152x=15,2\)
⇒ \(x=\dfrac{15,2}{152}=0,1\)
\(n_{AgNO3}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
500ml = 0,5l
\(C_{M_{ddAgNO3}}=\dfrac{0,2}{0,5}=0,4\left(M\right)\)
Chúc bạn học tốt

bài 3
Cu +2 AgNO3 -> Cu(NO3)2 + 2Ag
x...............2x.................................2x (mol)
theo bài ta có : 216x-64x=152x=2,28
==> x=0,015 (mol)=> n AgNO3=2x=0,03
==> CMAgNO3 =\(\dfrac{0,03}{\dfrac{30}{1000}}=1\left(M\right)\)
vậy............
bài 1
Zn + CuSO4 -> ZnSO4 + Cu
x x x (mol)
theo bài có 161x-160x=0,2==> x=0,2 = nZn
==> mZn tham gia = 0,2.65=13 (g)
vậy.........

a) mdd CuSO4 = 25.1,12 = 28 (g)
=> \(m_{CuSO_4}=\dfrac{28.15}{100}=4,2\left(g\right)\)
PTHH: Fe + CuSO4 --> FeSO4 + Cu
_____a----->a---------->a--------->a
=> 2,5 + 64a - 56a = 2,58
=> a = 0,01 (mol)
=> mCuSO4 dư = 4,2 - 0,01.160 = 2,6 (g)
b) mdd sau pư = 28 + 0,01.56 - 0,01.64 = 27,92(g)
\(\left\{{}\begin{matrix}C\%\left(CuSO_4\right)=\dfrac{2,6}{27,92}.100\%=9,3\%\\C\%\left(FeSO_4\right)=\dfrac{0,01.152}{27,92}.100\%=5,44\%\end{matrix}\right.\)
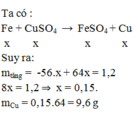

có vài chỗ bị lỗi do hệ thống hoc24 nên bạn thông cảm nha:D
\n