Đốt cháy hoàn toàn 6,8 g một hợp chất vô cơ A. Sau phản ứng chỉ thu được 4,48 lít khí SO2 (đktc) và 3,6 g H2O, Lập CTHH của hợp chất A, biết tỉ khối của A so với H2 bằng 17.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{SO_2} = \dfrac{4,48}{22,4} = 0,2(mol)\\ n_{H_2O} = \dfrac{3,6}{18} = 0,2(mol) \)
BTKL :
\(m_{O_2} = m_{SO_2} + m_{H_2O} - m_A = 0,2.64 + 3,6-6,8=9,6(gam) \\ \Rightarrow n_{O_2} = 0,3\ mol\)
BTNT với O :
\(n_O = 2n_{SO_2} + n_{H_2O} - 2n_{O_2} = 0,2.2 + 0,2 - 0,3.2 = 0\).Chứng tỏ A không chứa oxi.
\(n_S = n_{SO_2} = 0,2\ mol\\ n_H = 2n_{H_2O} = 0,4\ mol\)
Ta có :
\(n_S : n_H = 0,2 : 0,4 = 1 : 2\)
Vậy CTHH của A : H2S

ban oi online math la de giai toan chu khong phai hoa hoc nha

Gọi CTĐGN của A là \(C_xH_y\)
\(n_{CO_2}=\dfrac{4,48}{22,4}=0,2mol\Rightarrow m_C=0,2\cdot12=2,4g\)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3mol\Rightarrow n_H=2n_{H_2O}=0,6mol\Rightarrow m_H=0,6g\)
\(\Rightarrow x:y=n_C:n_H=0,2:0,6=1:3\)
\(\Rightarrow\left\{{}\begin{matrix}x=1\\y=3\end{matrix}\right.\)\(\Rightarrow CTĐGN\) là \(CH_3\)
Gọi CTHH cần tìm là \(\left(CH_3\right)_n\)
Theo bài: \(M_A=15\cdot2=30g\)\(\Rightarrow15n=30\Rightarrow n=2\)
Vậy A cần tìm có CTHH là \(C_2H_6\)

$M_A = 30.2 =60(g/mol)$
$n_{CO_2} = \dfrac{4,48}{22,4} = 0,2(mol)$
$n_{H_2O} = \dfrac{3,6}{18} = 0,2(mol)$
Bảo toàn nguyên tố C,H :
$n_C = n_{CO_2} = 0,2(mol) ; n_H =2 n_{H_2O} = 0,4(mol)$
$\Rightarrow n_O = \dfrac{6 - 0,2.12 - 0,4}{16} = 0,2(mol)$
$n_C: n_H : n_O = 0,2 : 0,4 : 0,2 = 1 : 2 : 1$
Suy ra : CT của A là $(CH_2O)_n$
$M_A = 30n = 60 \Rightarrow n =2 $
Vậy CT của A là $C_2H_4O_2$

2
nCO2 = 6,72/22,4=0,3 mol
=> nC = 0,3 mol
nH2O= 7,2/18=0,4 mol
=> nH= 0,4.2=0,8 mol
=> nC : nH = 0,3 : 0,8 = 3 : 8
=> CTĐG của hợp chất hữu cơ là (C3H8)n
Ta có: M CxHy= 1,517 x 29 = 44 (g/mol)
=>. 44n = 44 => n=1
CTHH của hợp chất hữu cơ là C3H8

a, Đốt A thu SO2 và H2O → A gồm S và H, có thể có O.
Ta có: \(n_S=\dfrac{25,6}{64}=0,4\left(mol\right)=n_S\)
\(n_{H_2O}=\dfrac{7,2}{18}=0,4\left(mol\right)\Rightarrow n_H=0,4.2=0,8\left(mol\right)\)
⇒ mS + mH = 0,4.32 + 0,8.1 = 13,6 (g) = mA
Vậy: A chỉ gồm S và H.
Gọi CTHH của A là SxHy.
\(\Rightarrow x:y=0,4:0,8=1:2\)
Vậy: CTHH của A là H2S.
b, - Đốt X thu P2O5 và H2O. → X gồm P và H, có thể có O.
Ta có: \(n_{P_2O_5}=\dfrac{14,2}{142}=0,1\left(mol\right)\Rightarrow n_P=0,1.2=0,2\left(mol\right)\)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\Rightarrow n_H=0,3.2=0,6\left(mol\right)\)
⇒ mP + mH = 0,2.31 + 0,6.1 = 6,8 (g) = mX
Vậy: X chỉ gồm P và H.
Gọi CTHH của X là PxHy.
⇒ x:y = 0,2:0,6 = 1:3
Vậy: CTHH của X là PH3.
c, Đốt Y thu CO2 và H2O → Y gồm C và H, có thể có O.
Ta có: \(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{2,7}{18}=0,15\left(mol\right)\Rightarrow n_H=0,15.2=0,3\left(mol\right)\)
⇒ mC + mH = 0,1.12 + 0,3.1 = 1,5 (g) < mY
→ Y gồm C, H và O.
⇒ mO = 2,3 - 1,5 = 0,8 (g) \(\Rightarrow n_O=\dfrac{0,8}{16}=0,05\left(mol\right)\)
Gọi CTHH của Y là CxHyOz.
⇒ x:y:z = 0,1:0,3:0,05 = 2:6:1
→ Y có CTHH dạng (C2H6O)n
\(\Rightarrow n=\dfrac{46}{12.2+6+16}=1\)
Vậy: CTHH của Y là C2H6O.

nCO2 = \(\dfrac{6,72}{22,4}\)= 0,3 mol , nH2O = \(\dfrac{5,4}{18}\)= 0,3 mol
=> mC = 0,3.12 = 3,6 gam , mH = 2nH2O . 1 = 0,6gam
mC + mH = 4,2g < mA => Trong A ngoài C và H còn có Oxi
mO = 5,8 - 4,2 = 1,6 gam <=> nO = 1,6/16 = 0,1 mol
Gọi CTĐGN của A là CxHyOz
Ta có x:y:z = nC:nH:nO = 3:6:1 => CTPT của A là (C3H6O)n
2,32 g A có thể tích = 1/3 thể tích 1,92 gam O2 ở cùng điều kiện
=> 2,32 g A có số mol = 1/3 số mol của 1,92 gam O2 = \(\dfrac{1,92}{32.3}\)= 0,02mol
<=> MA = \(\dfrac{2,32}{0,02}\)= 116(g/mol)
=> n = 2 và CTPT của A là C6H12O2
b) B tác dụng được với KOH, CaCO3 => B là axit cacboxylic
CH3-(CH2)4-COOH

MA= 1,0625*32 = 34 g/mol (1)
Vì đốt khí A thu dc SO2 va2H2O -> A chứa S, H
nS= 2,24/22,4=0,1 mol
nH= 2nH2O= 2*(1,8/18)=0,2 mol
nH : nS = 0,2 :0,1 =2:1 (2)
(1)(2)=> A là H2S
2H2S + 3O2 -> 2SO2 + 2H2O
0,1 0,15
nH2S= 3,4/34=0,1 mol
VO2= 0,15*22,4=3,36 l
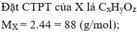
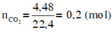
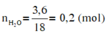

Ta có:
\(\left\{{}\begin{matrix}n_{SO2}=\frac{4,48}{22,4}=0,2\left(mol\right)\\n_{H2O}=\frac{3,6}{18}=0,2\left(mol\right)\end{matrix}\right.\)
BTNT H , S :
\(\Rightarrow m_H+m_S=0,2.2.1+0,2.32=6,8\left(g\right)\)
=> A chỉ có H và S
Tỉ lệ : \(\frac{n_H}{n_S}=\frac{0,4}{0,2}=\frac{2}{1}\)
Nên công thức đơn giản nhất : (H2S)n
\(\Leftrightarrow n\left(2+32\right)=17.2\)
\(\Leftrightarrow n=1\)
Vậy công thức hóa học của A là H2S