Cho 1 lít dung dịch CuCl2 0,1M. Điện phân với cường độ 10A trong vòng 2895s. Khối lượng Cu thoát ra là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
Ta có:

![]()
Ta có quá trình xảy ra tại các điện cực:
Catot Anot
![]()
![]()
0,08 → 0,16 0,01 → 0,04
Nhận thấy: ![]() chưa điện phân hết
chưa điện phân hết
Bảo toàn electron ta có: n C u = 1 2 n e n h ậ n = 0 , 02 m o l → m c a t o t t ă n g = m C u = 0 , 02 . 64 = 1 , 28 g

Đáp án A.
Theo định luật II của Pha – ra – đây thì khối lượng Cu sinh ra ở catot là:
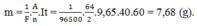

Đáp án C
Nhận thấy khối lượng dung dịch giảm không tỉ lệ với thời gian, ở anot luôn thu được O2 do vậy khối lượng chênh lệch là do Mn+ hết và bị thay thế bằng quá trình điện phân H2O tạo H2.
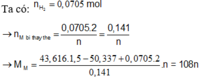
thỏa mãn n=1 thì M là Ag
Tại thời gian t giây gọi số mol Ag bị điện phân là x, suy ra n O 2 = 0 , 25 x
→ 108x+32.0,25x = 43,616 → x = 0,376
→ n A g N O 3 = 0,376.1,5 - 0,0705.2 = 0,423
→ m = 71,91 gam


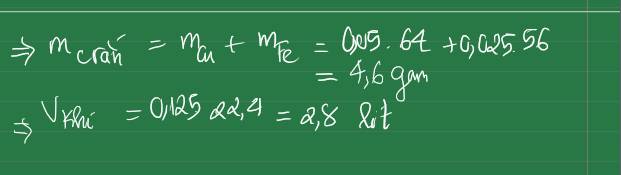



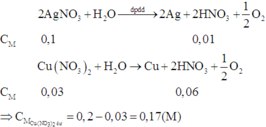

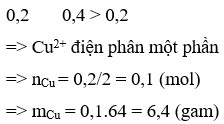
Số mol electron trao đổi là : \(\frac{10.2895}{96500}=0,3\left(mol\right)\)
\(n_{Cu^{2+}}=n_{CuCl2}=0,1.1=0,1\left(mol\right)\)
Vì \(n_e>2n_{CuCl2}\)nên Cu2+ hết
\(n_{Cu}=n_{CuCl2}=0,1\left(mol\right)\)
\(\Rightarrow m_{Cu}=0,1.64=6,4\left(g\right)\)