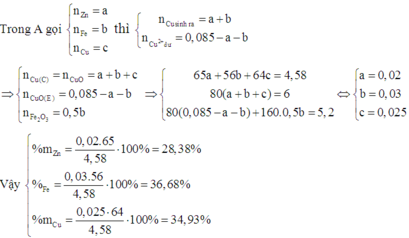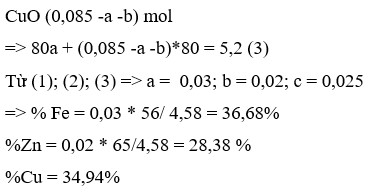Cho 27,4 gam bari vào 400 gam dung dịch CuSO4 3,2% , thu được khí A , kết tủa B và dung dịch C.
1. Tính thể tích khí A (đktc) và xác định kết tủa B gồm những chất nào.
2. Nung kết tủa B ở nhiệt độ cao đến khối lượng không đổi thì thu được bao nhiêu gam chất rắn?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Pt: Ba+2H2O -> Ba(OH)2+H2 (1)
Ba(OH)2+CuSO4 ->Cu(OH)2 \(\downarrow\) +BaSO4 \(\downarrow\)(2)
Ba(OH)2+(NH4)2SO4 ->BaSO4 \(\downarrow\)+2NH3+2H2O (3)
Cu(OH)2\(\underrightarrow{t^0}\)CuO+H2O (4)
BaSO4 \(\underrightarrow{t^0}\) ko xảy ra phản ứng
Theo (1) ta có \(n_{H_2}=n_{Ba\left(OH\right)_2}=n_{Ba}=\frac{27,4}{137}=0,2\left(mol\right)\)
\(n_{\left(NH_4\right)_2SO_4}=\frac{1,32\cdot500}{132\cdot100}=0,05\left(mol\right)\)
\(n_{CuSO_4}=\frac{2\cdot500}{100\cdot160}=0,0625\left(mol\right)\)
Ta thấy: \(n_{Ba\left(OH\right)_2}>n_{\left(NH_4\right)_2SO_4}+n_{CuSO4\:}\) nên Ba(OH)2 dư và 2 muối đều phản ứng hết
Theo (2) ta có: \(n_{Ba\left(OH\right)_2}=n_{Cu\left(OH\right)_2}=n_{BaSO_4}=n_{CuSO_4}=0,0625\left(mol\right)\)
Theo (3) ta có: \(n_{Ba\left(OH\right)_2}=n_{BaSO_4}=n_{\left(NH_4\right)_2SO_4}=0,05\left(mol\right)\)
và \(n_{NH_3}=2n_{\left(NH_4\right)_2SO_4}=0,05\cdot2=0,1\left(mol\right)\)
\(\Rightarrow n_{Ba\left(OH_2\right)}\text{dư}=0,2-\left(0,05+0,0625\right)=0,0875\left(mol\right)\)
a)\(V_{A\left(ĐKTC\right)}=V_{H_2}+V_{NH_3}=\left(0,2+0,1\right)\cdot22,4=6,72\left(l\right)\)
b)Theo (4) ta có: \(n_{CuO}=n_{Cu\left(OH\right)_2}=0,0625\left(mol\right)\)
\(m_{\text{chất rắn}}=m_{BaSO_4}+m_{CuO}=\left(0,0625+0,05\right)\cdot233+0,0625\cdot80=31,2125\left(g\right)\)

mCuSO4= 12,8(g) ->nCuSO4=0,2(mol)
nNa=0,04(mol)
pthh: Na + H2O -> NaOH + 1/2 H2
-> nNaOH= 0,04(mol); nH2=0,02(mol)
=> V(A,đktc)=V(H2,đktc)=0,02.22,4=0,448(l)
2 NaOH + CuSO4 -> Cu(OH)2 + Na2SO4
Ta có: 0,04/2 < 0,2/1
=> CuSO4 dư, NaOH hết, tính theo nNaOH
=> nCu(OH)2=nCuSO4(p.ứ)=nNa2SO4=nNaOH/2=0,02(mol)
=> m(B)=mCu(OH)2=0,02.98=1,96(g)
b) mddC=mddCuSO4 + mNaOH - mCu(OH)2= 400+ 0,04.40- 1,96= 399,64(g)
mCuSO4(dư)= 0,18 x 160=28,8(g)
mNa2SO4=0,02.142= 2,84(g)
=> C%ddCuSO4(dư)= (28,8/399,64).100=7,206%
C%ddNa2SO4=(2,84/399,64).100=0,711%

nBa = \(\frac{54,8}{137}\) = 0,4 (mol)
nCuSO4 = \(\frac{800.3,2\%}{160}\) = 0,16 (mol)
Ba + 2 H2O \(\rightarrow\) Ba(OH)2 + H2 \(\uparrow\)
0,4 -------------> 0,4 ------> 0,4 (mol)
Ba(OH)2 + CuSO4 \(\rightarrow\) BaSO4 \(\downarrow\) + Cu(OH)2 \(\downarrow\)
bđ 0,4 .......... 0,16 (mol)
pư 0,16 <------ 0,16 -----> 0,16 ------> 0,16 (mol)
spư 0,24 ....... 0 .............. 0,16 .......... 0,16 (mol)
Khí A : H2 : 0,4 mol
Kết tủa B: \(\begin{cases}BaSO_4:0,16mol\\Cu\left(OH\right)_2:0,16mol\end{cases}\)
dd C: Ba(OH)2 : 0,24 mol
a)VH2 = 0,4 . 22,4 = 8,96 (mol)
b) Cu(OH)2 \(\underrightarrow{t^0}\) CuO + H2O
0,16 ------------> 0,16 (mol)
CR thu đc sau pư: \(\begin{cases}BaSO_4:0,16mol\\CuO:0,16mol\end{cases}\)
mCR = 0,16 . 233 + 0,16 . 80 = 50,08 (g)
c) mdd = 54,8 + 800 - 0,4 . 2 - 50,08 = 803,92 (g)
C%(Ba(OH)2)= \(\frac{0,24.171}{803,92}\) . 100% = 5,1%

Đáp án A
m = m BaSO 4 + m Cu ( OH ) 2 = 233 ( 0 , 05 + 0 , 0625 ) + 98 . 0 , 0625 = 32 , 3375 ( gam )

Đáp án A
Các phản ứng có thể xảy ra:
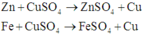
Trong 3 kim loại Zn, Fe và Cu thì Fe có khối lượng mol nhỏ nhất
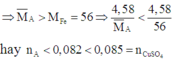
Do đó B chứa Cu2+ dư
Khi đó C chứa Cu trong A và Cu sinh ra sau phản ứng. Nên D chứa CuO.
B chứa Zn2+, Fe2+ và Cu2+ dư. Khi cho B tác dụng với dung dịch NaOH dư thì kết tủa thu được chứa Fe(OH)2 và Cu(OH)2 .
Do đó E chứa Fe2O3 và CuO.