Điện phân một muối clorua kim loại kiềm nóng chảy thu được 1,68 lit khí clo ( đkc) ở anot và 5,85g kim loại ở catot. Công thức muối đó là :
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


CTHH: AClx
\(n_{Cl_2}=\dfrac{1,42}{71}=0,02\left(mol\right)\)
2AClx --đp-->2 A + xCl2
_________\(\dfrac{0,04}{x}\) <-0,02
=> \(M_A=\dfrac{1,56}{\dfrac{0,04}{x}}=39x\left(g/mol\right)\)
Xét x = 1 => MA = 39(K)
=> CTHH: KCl
=> B

CT muối clorua của KL kiềm là MCl
2MCl -dpnc→ 2M + Cl2
Khí ở anot là Cl2. Số mol Cl2: 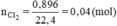
Số mol M là: nM = 0,04. 2 = 0,08 (mol)
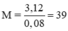 → M là K
→ M là K
Công thức muối KCl

Đáp án A
Gọi công thức của muối kim loại kiềm là RCl
- Phản ứng: 2RCl → t o 2R + Cl2
nCl2 = 0,896: 22,4 = 0,04 mol => nR = 2nCl2 = 0,08 mol
=> MR = 3,12: 0,08 = 39 g/mol => Kali => Muối là KCl

TK
CT muối clorua của KL kiềm là MCl
2MCl -dpnc→ 2M + Cl2
Khí ở anot là Cl2. Số mol Cl2:
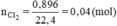
Số mol M là: nM = 0,04. 2 = 0,08 (mol)
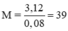
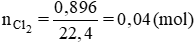
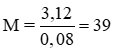 → M là K
→ M là K

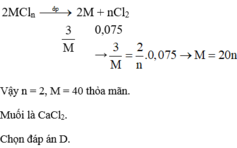
\(2MCl_n\rightarrow2M+nCl_2\)
Ta có :
\(n_{Cl2}=\frac{1,68}{22,4}=0,075\left(mol\right)\)
\(\Rightarrow n_M=\frac{0,075.2}{n}=\frac{0,15}{n}\left(mol\right)\)
\(\Rightarrow M_M=\frac{5,85}{\frac{0,15}{n}}=39n\left(\frac{g}{mol}\right)\)
\(\Rightarrow n=1\Rightarrow M_M=39\left(\frac{g}{mol}\right)\)
\(\Rightarrow M:Kali\left(K\right)\)
Vậy CTHH của muối là KCl
\(2MCl-->2M+Cl2\)
\(n_{C_{ }l2}=\frac{1,68}{22,4}=0,075\left(mol\right)\)
\(n_M=2n_{Cl2}=0,15\left(mol\right)\)
\(M_M=\frac{5,85}{0,15}=39\left(K\right)\)
Vậy M là Kali