Hỗn hợp X chứa hai muối KX và KY (X,Y là các halogen thuộc hai chu kì kế tiếp nhau Mx < My) tác dụng với lượng dư đe Agno3 sau p/ứ thu đc 16,575 gam kết tủa. Biết rằng khi phân hủy lượng kết tủa trên thu được 10,8 gam kết tủa. Công thức của muối KY là?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án C
Gọi công thức chung của NaX và NaY là NaM.
NaM + AgNO3 → AgM↓+NaNO3
0,03 →0,03 (mol)
![]()
=> M = 50,3 => X,Y lần lượt là Cl và Br

Chọn A
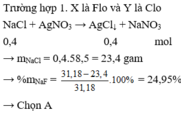
Chú ý: Với đề trắc nghiệm chọn được đáp án A có thể không cần xét thêm trường hợp 2.
Trường hợp 2. X khác Flo. Gọi hỗn hợp (NaX, NaY) tương đương với NaM


- Nếu chỉ một trong hai muối tác dụng với Bạc nitrat :
Suy ra hai muối là NaCl và NaF
\(AgNO_3 + NaCl \to AgCl + NaNO_3\\ n_{NaCl} = n_{AgCl} = \dfrac{43,2}{143,5} = 0,3(mol)\\ \Rightarrow m_{NaCl} = 0,3.58,5 = 17,55 < 25,3(\text{thỏa mãn})\)
- Nếu cả hai muối đều tác dụng với Bạc nitrat :
Gọi CTTQ của hai muối : NaX
\(NaX + AgNO_3 \to AgX + NaNO_3\\ n_{NaX} = n_{AgX} \\ \Leftrightarrow \dfrac{25,3}{23 + X} = \dfrac{43,2}{108+X}\\ \Rightarrow X = 97,13\\ M_{Br} = 80 < M_X = 97,13 < M_I = 127\)
Vậy hai muối là NaBr và NaI

MCl + AgNO3 -> AgCl + MNO3 (M là hai kim loại kiềm)
mol: 0,13 0,13
Ta có : (M+35,5).0,13 = 6,645
=> M = 15,62
Hai kim loại kiềm trên là Li và Na.
=> Đáp án D

+) Trường hợp 1: Hỗn hợp gồm NaF và NaCl
PTHH: \(NaCl+AgNO_3\rightarrow AgCl\downarrow+NaNO_3\)
Ta có: \(n_{AgCl}=\dfrac{2,87}{143,5}=0,02\left(mol\right)=n_{NaCl}\)
\(\Rightarrow m_{NaCl}=0,02\cdot58,5=1,17\left(g\right)\) \(\Rightarrow m_{NaF}=0,415\left(g\right)\)
+) Trường hợp 2: Hỗn hợp không chứa NaF
Gọi công thức chung 2 muối là NaR
PTHH: \(NaR+AgNO_3\rightarrow NaNO_3+AgR\downarrow\)
Theo PTHH: \(n_{NaR}=n_{AgR}\) \(\Rightarrow\dfrac{1,595}{23+\overline{M}_R}=\dfrac{2,87}{108+\overline{M}_R}\)
\(\Rightarrow\overline{M}_R\approx83,3\) \(\Rightarrow\) 2 halogen cần tìm là Brom và Iot
Vậy 2 muối có thể là (NaF và NaCl) hoặc (NaBr và NaI)
*P/s: Các phần còn lại bạn tự làm

a)
Gọi công thức chung là KR
\(KR+AgNO_3\rightarrow AgR+KNO_3\)
\(n_{AgR}=\frac{25,145}{108+R}\)
\(n_{KR}=\frac{17,21}{39+R}\)
Ta có :\(n_{AgR}=nKR\)
\(\Leftrightarrow\frac{25,145}{108+R}\Leftrightarrow\frac{17,21}{39+R}\)
\(\Rightarrow R=110,65\)
\(\Rightarrow Br< R< I\Rightarrow\) X là Br ,Y là I
b)
\(KBr+AgNO_3\rightarrow AgBr+KNO_3\)
a__________________a______
\(KI+AgO_3\rightarrow AgI+KNO_3\)
b_____________b______________
Giải hệ PT:
\(\left\{{}\begin{matrix}119a+166b=17,21\\188a+235b=25,145\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,04\\b=0,075\end{matrix}\right.\)
\(\%m_{KBr}=\frac{0,04.119.100}{17,21}=27,65\%\)
\(\%m_{KI}=100\%-27,65\%=72,35\%\)
c)
\(2KBr+Cl_2\rightarrow2KCl+Br_2\)
x_____x/2 ____x_______
\(2KI+Cl_2\rightarrow2KCl+I_2\)
y_____ y/2 ____ y
Ta có hệ PT:
\(\left\{{}\begin{matrix}119x+166y=17,21\\x+y=\frac{9,68}{74,5}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,09\\y=0,04\end{matrix}\right.\)
\(V_{Cl2}=\left(\frac{0,09}{2}+\frac{0,04}{2}\right).22,4=1,456\left(l\right)\)




- TH1: KX , KY cùng tạo kết tủa
\(n_{Ag}=\frac{10,8}{108}=0,1\left(mol\right)\)
Gọi chung kết tủa là AgR
\(2AgR\underrightarrow{^{to}}2Ag+R_2\)
0,1_______0,1_________
\(\Rightarrow\overline{M_{AgR}}=\frac{16,575}{0,1}=165,75\) (I và At)
Nên KY là KAt
- TH2 : KX là KF ( không tạo kết tủa )
Nên KY là KCl
\(2AgCl\rightarrow2Ag+Cl_2\)
0,1______0,1_______
\(\Rightarrow M_{AgCl}=\frac{16,575}{0,1}=165,75\ne143,5\) (loại)