Cho 23,5g hỗn hợp 2 kim loại đứng trước hiđro tác dụng vừa đủ với dd HCl thu được 12,32 lít H2 (đktc) và dd Y. Cô cạn dd Y thu được khối lượng muối khan là bao nhiêu ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


n H2=0,55=> n HCl=1,1=> m cl=36.05
m khô cạn = m Cl+m KL=62.55 g
sai thì thôi

Đáp án A
Chất rắn Y là Cu không phản ứng
nHCl = ![]() = 2.0,35 = 0,7
= 2.0,35 = 0,7
mmuối = mKL + mgốc axit = (9,14 – 2,54) + 0,7.35,5 = 31,45(g)

\(n_{Zn}=a\left(mol\right),n_{Al}=b\left(mol\right)\)
\(n_{H_2}=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+H_2\)
\(n_{H_2}=a+1.5b=0.4\left(mol\right)\left(1\right)\)
\(m_{Muối}=m_{ZnCl_2}+m_{AlCl_3}=136a+133.5b=40.3\left(g\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.1,b=0.2\)
\(m_{hh}=0.1\cdot65+0.2\cdot27=11.9\left(g\right)\)
\(\%Zn=\dfrac{0.1\cdot65}{11.9}\cdot100\%=54.62\%\)
\(\%Al=100-54.62=45.38\%\)

a, nHCl = 0,27 ( mol )
=> n(H) = 0,27 ( mol )
=> nH2 = 0,135 ( mol )
=> VH2 = 3,024 ( l )
b, Có n(Cl) = nHCl = 0,27 ( mol )
=> m(Cl) = 9,585 ( g )
=> mMuối = mKl + m(Cl) = 3,88 + 9,585 = 13,465 ( g )
nHCl = 0,135.2 = 0,27 mol
Phản ứng vừa đủ , áp dụng ĐLBT nguyên tố H => nH2 = \(\dfrac{0,27}{2}\)=0,135mol
=> V H2 = 0,135. 22,4 = 3,024 lít
b) Hỗn hợp kim loại + HCl --> Hỗn hợp muối + H2
Áp dụng ĐLBT khối lượng => m hh kim loại + m HCl = m hỗn hợp muối + mH2
=> m muối = 3,88 + 0,27.36,5 - 0,135.2 =13,465 gam

nO2=0,085(mol) => nO= 0,17(mol)
m hỗn hợp KL=3,36(g)
nO(trong H2O) = nO(trong O2) = 0,17
=> nH2O = 0,17
=> nH(trong HCl) = nH(trong H2O) = 2nH2O= 0,34
=> nHCl=0,34
=> nCl= 0,34
m muối khan= mKL + mCl = 3,36 + 0,34 x 35,5 = 15,43
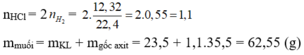

Cả 2 kim loại đều phản ứng với HCl do đứng trước H
23,5 kim loại + HCl (vừa đủ) \(\rightarrow\) Y (muối ) + H2
\(n_{H2}=0,55\left(mol\right)\)
Ta có : \(2HCl\rightarrow1H_2\)
Bảo toàn nguyên tố H : \(n_{HCl}=2n_{H2}=1,1\left(mol\right)\)
BTKL ,
\(m_{kl}+m_{HCl}=m_{Muoi}+m_{H2}\)
\(\Leftrightarrow23,5+1,1.36,5=m_{muoi}+0,55.2\Leftrightarrow m_{muoi}=62,55\left(g\right)\)
\(PTTQ\): \(M+2HCl-->MCl2+H2\)
\(n_{H2}=\frac{12,32}{22,4}=0,55\left(mol\right)\)
\(m_{H2}=0,55.2=1,1\left(g\right)\)
\(n_{HCl}=2n_{H2}=1,1\left(mol\right)\)
\(m_{HCl}=1,1.36,5=40,15\left(g\right)\)
\(m_{muối}=m_{KL}+m_{HCl}-m_{H2}\)
\(=23,5+40,15-1,1=62,55\left(g\right)\)