Cho 100ml dung dịch NaBr 1,2M vào dung dịch chứa 200 gam dung dịch AgNO3 8,5%. Sau phản ứng hoàn toàn thu được m gam kết tủa. Tính m?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B
Chú ý đổ từ từ muối Na2CO3 và NaHCO3 vào dung dịch H2SO4 thì xảy ra đồng thời các phương trình
2H+ + CO32- → CO2 + H2O (1)
2x------> x
H+ + HCO3- → CO2 + H2O (2)
y -----> y
Ta có 2x+ y = 0,2 mol
Vì phản ứng xảy ra đồng thời nên x: y = nCO32- : nHCO3- = 0,12 : 0,06 = 2:1
Ta có hệ: 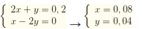
Vậy dung dịch X chứa : HCO3- dư : 0,02 mol, CO32- :0,04 mol
Khi cho dung dịch BaCl2 vào dung dịch X thì nBaCO3 = nCO32- = 0,04 mol → mkết tủa = 7,88 gam. Đáp án B

Chọn B.
Dung dịch X chứa Mg(NO3)2 và Cu(NO3)2 . Khi cho X tác dụng với Fe thì:
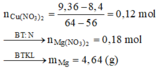

Dung dịch X chứa Mg(NO3)2 (a mol) và Cu(NO3)2 dư (b mol)
Bảo toàn N => 2a + 2b = 0,1 + 0,25.2
X với Fe: ∆ m = 64b - 56b = 9,36 - 8,4
Giải hệ được a = 0,18 và b = 0,12
Trong 19,44 gam kết tủa chứa Ag (0,1), Cu
(0,25 - 0,12 = 0,13) => mMg dư = 0,32
m = 0,18.24 + 0,32 = 4,64
Đáp án C

Đáp án : D
Dung dịch X chứa 2 muối chắc chắn là Cu2+ và Mg2+
Trong kết tủa có thể có Mg chưa kịp phản ứng với Cu2+
Thêm 4,2g Fe và thu được 4,68g > mFe => Phản ứng với Cu2+
=> nCu2+ = (4,68 – 4,2)/(64 – 56) = 0,06 mol
=> Dung dịch muối có 0,09 mol Mg2+ ; 0,06 mol Fe2+(bảo toàn điện tích với NO3-)
Bảo toàn khối lượng :
, m + mAgNO3 + Cu(NO3)2 = mKết tủa + mdd X
,mdd X + mFe = mrắn + mdd sau
=> m = 2,32g




\(n_{NaBr}=1,2.0,1=0,12\left(mol\right)\)
\(m_{AgNO3}=\frac{8,5.200}{100}=17\left(g\right)\)
\(n_{AgNO3}=\frac{17}{170}=0,1\left(mol\right)\)
\(PTHH:NaBr+AgNO_3\rightarrow NaNO_3+AgBr\downarrow\)
Lập tỉ lệ: \(\frac{0,12}{1}>\frac{0,1}{1}\Rightarrow\)NaBr dư, AgNO3 hết
\(n_{AgBr}=n_{AgNO3}=0,1\left(mol\right)\)
\(\Rightarrow m_{AgBr}=0,1.188=18,8\left(g\right)\)