cho 6,72 lít khí Cl2(ddktc) qua 400ml dung dịch NaBr 2M,sau phản ứng thu được dung dịch X.Cô cạn dung dịch X thu được m gam muối khan, tính m ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{Cl_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(n_{NaBr}=0.5\left(mol\right)\)
\(2NaBr+Cl_2\rightarrow2NaCl+Br_2\)
\(0.4..........0.2...........0.4........0.2\)
\(m_X=m_{NaBr\left(dư\right)}+m_{NaCl}=\left(0.5-0.4\right)\cdot103+0.4\cdot58.5=33.7\left(g\right)\)

\(n_{Cu}=0,125\left(mol\right);n_{NaNO_3}=0,15;n_{H_2SO_4}=0,15\left(mol\right)\)
PT ion: 3Cu + 2NO3- + 8H+ → 3Cu2+ + 2NO + 4H2O
BĐ: 0,125.........0,15..........0,3
PU : 0,1125......0,075..........0,3...........0,1125........0,075..........0,15
Dư: 0,0125.......0,075...........0
=> \(V_{NO}=0,075.22,4=1,68\left(l\right)\)
Muối tạo thành : Cu2+, SO42-, Na+, NO3- dư
=> \(m_{muối}=m_{Cu^{2+}}+m_{SO_{\text{4}}^{2-}}+m_{Na^+}+m_{NO_3^-\left(dư\right)}=0,1125.64+0,15.96+0,15.23+0,075.62=29,7\left(g\right)\)

NaOH + HCl --> NaCl+H2O (1)
2NaOH +H2SO4 --> Na2SO4 +2H2O (2)
Đặt nNaOH (1)= a(mol)
nNaOH(2) = b (mol)
=>a + b = 0,3.2 =0,6( *)
Theo PT (1) : nNaCl = nNaOH(1) = a(mol)
Theo PT (2) : nNa2SO4=12
nNaOH(2) = 0,5b(mol)
=>58,5a + 71b =40,1(**)
Từ (*), (**) => a= 0,2 ; b = 0,4
nHCl = nNaOH (1)=0,2 mol
=> x=CMHCl=0,20,2=1M
nH2SO4 = nNaOH (2)=0,4 mol
y=CMH2SO4=0,40,2=2M

Ta có phương trình ion tổng quát sau : CO32- + 2H+ → CO2 + H2O
=> n CO2 = nCO3 trong muối= 0,3 mol.
Ta thấy cứ 2 mol Cl- thay thế 1 mol CO3 2- trong muối
Vậy để thay thế 0,3 mol CO32- cần 0,6 mol Cl-
=> m muối sau phản ứng = m muối đầu + m Cl- - mCO32-
= 34,4 + 35,5.0,6 – 60.0,3 = 37,7g
=>D

nCO3 = 0,3 mol
=> nCl = 0,6
=> m = 34,4 - 0,3.60 + 0,6.35,5 = 37,7 => Đáp án D

Ta có phương trình ion tổng quát sau : CO32- + 2H+ → CO2 + H2O
=> n CO2 = nCO3 trong muối= 0,3 mol.
Ta thấy cứ 2 mol Cl- thay thế 1 mol CO3 2- trong muối
Vậy để thay thế 0,3 mol CO32- cần 0,6 mol Cl-
=> m muối sau phản ứng = m muối đầu + m Cl- - mCO32-
= 34,4 + 35,5.0,6 – 60.0,3 = 37,7g
=>D
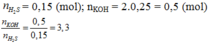
\(Cl_2+2NaBr\rightarrow2NaCl+Br_2\)
\(n_{Cl2}=\frac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{NaBr}=0,4.2=0,8\left(mol\right)\)
\(\Rightarrow n_{NaBr}=0,8-0,3.2=0,2\left(mol\right)\)
\(n_{NaCl}=0,3.2=0,6\left(mol\right)\)
\(\Rightarrow m=m_{NaBr}+m_{NaCl}=0,2.103+0,6.58,5=55,7\left(g\right)\)
nCl2=6,72\22,4=0,3 mol
nNaBr=0,8 mol
2NaBr+Cl2-->2NaCl+Br2
0,8\2=0,3
==>NaBrdư
=>mNaCl=0,3.58,5=17,55 g
=>mNaBr dư=0,1.103=10,3 g
=>mhh muối =17,55+51,5=27,85 g