Hòa tan hoàn toàn 9,36 gam hỗn hợp hai muối cacbonat của hai kim loại (nhóm IIA, hai chu kì liên
tiếp) vào dung dịch HCl dư, thu được 2,24 lít CO 2 (đktc). Hai kim loại và khối lượng muối trong dung dịch
thu được
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

n muối = n CO2 = 0,2 mol
--> PTK muối = 18,4/0,2 = 92
--> NTK kim loại = 92 - 60 = 32
Vì 24 < 32 < 40 --> hai kim loại là Mg và Ca

Gọi công thức muối cacbonat trung hòa của 2 kim loại kiềm cần tìm là R2CO3
\(R_2CO_3+2HCl\rightarrow2RCl+H_2O+CO_2\)
\(n_{CO_2}=n_{R_2CO_3}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ \Rightarrow M_{R_2CO_3}=2M_R+60=\dfrac{9,1}{0,1}=91\\ \Rightarrow M_R=15,5\)
Do 2 kim loại kiềm ở chu kì liên tiếp nhau
=> 2 kim loại đó là Li, Na

a) Gọi công thức chung của 2 kim loại là M
\(n_M=\dfrac{3,68}{M_M}\left(mol\right)\)
PTHH: M + 2HCl --> MCl2 + H2
\(\dfrac{3,68}{M_M}\)----------->\(\dfrac{3,68}{M_M}\)
=> \(\dfrac{3,68}{M_M}\left(M_M+71\right)=10,78\)
=> MM = 36,8(g)
Mà 2 kim loại liên tiếp nhau
=> 2 kim loại là Mg, Ca
Gọi số mol của Mg, Ca là a, b
=> 24a + 40b = 3,68
PTHH: Mg + 2HCl --> MgCl2 + H2
a----------------->a------>a
Ca + 2HCl --> CaCl2 + H2
b---------------->b------->b
=> 95a + 111b = 10,78
=> a = 0,02 ; b = 0,08
=> \(\left\{{}\begin{matrix}m_{Mg}=0,02.24=0,48\left(g\right)\\m_{Ca}=0,08.40=3,2\left(g\right)\end{matrix}\right.\)
b) VH2 = (a+b).22,4 = 2,24(l)

Đáp án: A
Ta có: nHCl= 2nH2 = 0,5 mol
m muối = m kim loại + mCl-
= 8,4 + 0,5. 35,5 = 26,15 gam


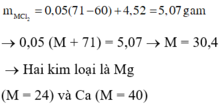
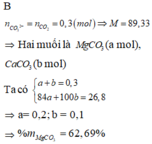


Gọi công thức chung của muối cacbonat là RCO3.
\(RCO_3+2HCl\rightarrow RCl_2+CO_2+H_2O\)
Ta có:
\(n_{RCO3}=n_{RCl2}=n_{CO2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
\(\Rightarrow M_{RCO3}=R+60=\frac{9,36}{0,1}=93,6\)
\(\Rightarrow R=33,6\Rightarrow24< 33,6< 40\)
Vậy 2 kim loại là Mg và Ca.
\(m_{RCl2}=0,1.\left(33,6+35,5.2\right)=10,46\left(g\right)\)