Hoà tan 3,1 gam Na2O vào trong nước thu được 1000 ml dung dịch NaOH.Nồng độ của dung dịch NAOH thu được là:
(1 Điểm)
0,005M
0,1M
0,05M
0,01M
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{NaOH}=\dfrac{4}{40}=0,1\left(mol\right)\\ C_{M_{NaOH}}=\dfrac{0,1}{0,4}=0,25\left(M\right)\)
n NaOH= \(\dfrac{4}{40}\)=0,1(mol)
C MnaoH=\(\dfrac{0,1}{0,4}\)=0,25(M)

Đáp án C
nNaOH (1) = 0,48 mol
nNaOH (2) = 0,51 mol
Gọi số mol A13+ trong m gam A1C13 là X
Coi 4a, 3a là số mol của Al(OH)3


TH1: Khi cho 0,48 mol NaOH thì chỉ tạo 1 phần kết tủa, khi cho 0,51 mol NaOH thì tạo kết tủa tối đa vào 1 phần bị tan
Trường hợp cho 0,51 mol NaOH
TH2: cả 2 lần đều tạo kết tủa tối đa và hòa tan 1 phần
Chênh lệch số mol kết tủa ở 2 trường hợp:
4
a
78
-
3
a
78
=
0
,
51
-
0
,
48
=
⇒
a
78
=
0
,
03
Trường hợp cho 0,48 mol NaOH
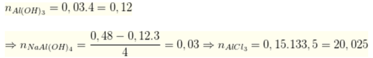
=>Đáp án C

Đáp án A
Từ giả thiết suy ra : Ở TN2 đã có hiện tượng hòa tan kết tủa. Còn ở TN1 thì có thể có hiện tượng hòa tan kết tủa hoặc chưa. Ta đặt :
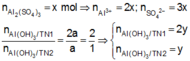
● Nếu cả TN1 và TN2 đều có hiện tượng hòa tan kết tủa, áp dụng bảo toàn điện tích cho các dung dịch sau phản ứng, ta có :
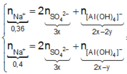
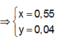
![]() thỏa mãn
thỏa mãn
Suy ra : ![]()
● Nếu TN1 chưa có hiện tượng hòa tan kết tủa, áp dụng bảo toàn điện tích cho các dung dịch sau phản ứng, ta có :
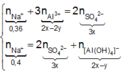
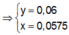
![]() (loại)
(loại)

a, \(Na_2O+H_2O\rightarrow2NaOH\)
Ta có: \(n_{Na_2O}=\dfrac{3,1}{62}=0,05\left(mol\right)\)
Theo PT: \(n_{NaOH}=2n_{Na_2O}=0,1\left(mol\right)\)
m dd sau pư = 3,1 + 50 = 53,1 (g)
\(\Rightarrow C\%_{NaOH}=\dfrac{0,1.40}{53,1}.100\%\approx7,53\%\)
b, \(2Na+2H_2O\rightarrow2NaOH+H_2\)
Ta có: \(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right)\)
Theo PT: \(\left\{{}\begin{matrix}n_{NaOH}=n_{Na}=0,2\left(mol\right)\\n_{H_2}=\dfrac{1}{2}n_{Na}=0,1\left(mol\right)\end{matrix}\right.\)
Ta có: m dd sau pư = 4,6 + 95,6 - 0,1.2 = 100 (g)
\(\Rightarrow C\%_{NaOH}=\dfrac{0,2.40}{100}.100\%=8\%\)

a)
C% CuSO4 = 16/(16 + 184) .100% = 8%
b)
n NaOH = 20/40 = 0,5(mol)
CM NaOH = 0,5/4 = 0,125M
1000 ml = 1 lít
$n_{Na_2O} = \dfrac{3,1}{62} = 0,05(mol)$
$Na_2O + H_2O \to 2NaOH$
$n_{NaOH} = 2n_{Na_2O} = 0,1(mol)$
$C_{M_{NaOH}} = \dfrac{0,1}{1} = 0,1M$