Cho dd halogen của kim loại R có hóa trị II phản ứng vừa đủ với bạc nitrat thu đc 5,74g kết tủa . Mặt khác, nếu nhúng thanh sắt vào lượng dd muối trên thì sau phản ứng khối lượng thanh sắt tăng thêm 0,16g. Xác định công thức hóa học của muối đã dùng.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Câu 1:
2M+nCuSO4\(\rightarrow\)M2(SO4)n+nCu
2M+nFeSO4\(\rightarrow\)M2(SO4)n+nFe
- Gọi a là số mol của M
- Độ tăng khối lượng PTHH1:
64na/2-Ma=20 hay(32n-M).a=20
- Độ tăng khối lượng PTHH2:
56.na/2-Ma=16 hay (28n-M)a=16
Lập tỉ số ta được:\(\dfrac{32n-M}{28n-M}=\dfrac{20}{16}=1,25\)
32n-M=35n-1,25M hay 0,25M=3n hay M=12n
n=1\(\rightarrow\)M=12(loại)
n=2\(\rightarrow\)M=24(Mg)
n=3\(\rightarrow\)M=36(loại)
Câu 2:Gọi A là khối lượng thanh R ban đầu.
R+Cu(NO3)2\(\rightarrow\)R(NO3)2+Cu
R+Pb(NO3)2\(\rightarrow\)R(NO3)2+Pb
- Gọi số mol Cu(NO3)2 và Pb(NO3)2 là x mol
- Độ giảm thanh 1: \(\dfrac{\left(R-64\right)x}{A}.100=0,2\)
- Độ tăng thanh 2: \(\dfrac{\left(207-R\right)x}{A}.100=28,4\)
Lập tỉ số: \(\dfrac{207-R}{R-64}=\dfrac{28,4}{0,2}=142\)
207-R=142R-9088 hay 143R=9295 suy ra R=65(Zn)

a) MH2+2AgNO3 ->M(NO3)2+2AgH
Fe+MH2 -> FeH2+M
gọi x là số mol của MH2 ở mỗi phần
x(M-56)=0,16=>x=0,16/(M-56)
=>nAgH=0,32/(M-56)
Ta có
mAgH=5,74=>0,32x(108+H)/(M-56)=5,74
=>(108+H)/(M-56)=17,9375
=>17,9375M-H=1112,5
thay H lần lượt là Cl , Br và I ta có
H là Cl thì M là Cu
=>CTHH của X là CuCl2
b)
ta có x(64-56)=0,16=>x=0,02 mol
=>mCuCl2=0,02x2x135=5,4 g

mR(NO3)2 = 500 . 15,04% = 75,2 (g)
Fe + R(NO3)2 → Fe(NO3)2 + R
1mo___1mol_______________ 1 mol tăng (MR -56)g
_____ x mol________________ tăng 103,2 - 100 = 3,2(g)
\(x=\frac{3,2}{M_R-56}\)
\(m_{R\left(NO3\right)2}=\frac{3,2}{M_R-56}.\left(M_R+124\right)=75,2\)
\(\rightarrow M_R=64\)
→ R là đồng (Cu)
→ Muối nitrat: Cu(NO3)2
mR(NO3)2=3,2/MR-56.(MR+124)=75,2 tại sao lại suy ra MR =64 ạ giải thích hộ em với ạ

a , \(nFe=\dfrac{11,2}{56}=0,2\left(mol\right)\)
, pthh:
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
1mol 2mol 1mol 1mol
0,2 0,4 0,2 0,2
\(FeCl_2+2NaOH\rightarrow Fe\left(OH\right)_2\downarrow+2NaCl\)
1mol 2mol 1mol 2mol
0,2 0,4 0,2 0,4
b, \(mFe\left(OH\right)_2=0,2.90=18\left(gam\right)\)



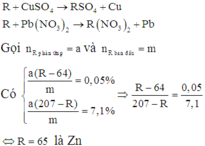
\(RX_2+2AgNO_3\rightarrow2AgX+R\left(NO_3\right)_2\)
\(Fe+RX_2\rightarrow R+FeCl_2\)
\(n_{AgX}=\frac{5,74}{108+M_X}\left(mol\right)\)
\(n_{Fe}=n_R=\frac{2,87}{108+M_X}\left(mol\right)\)
\(M_R.\frac{2,87}{108+M_X}-56.\frac{1,87}{108+M_X}=0,16\)
\(M_R.2,87-160,72=17,28+0,16M_X\)
\(\Rightarrow M_X=35,5M_R=64\)
Vậy X là Cl , R là Cu
Công thức hóa học là CuCl2