Câu 4. Cho 0,88 gam hỗn hợp gồm hai kim loại kiềm thổ ở hai chu kỳ liên tiếp tác dụng hết với dung dịch HCl dư, sau phản ứng thu được 0,672 lít khí H2 (đktc). a. Xác định 2 kim loại trên? b. Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp trên?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chọn C
Các chất thỏa mãn : Al2O3 ; Zn(OH)2 ; NaHS ; (NH4)2CO3 ; Al

Đáp án : C
Tổng quát : M + 2H2O -> M(OH)2 + H2
=> nM = nH2 = 0,3 mol => Mtb = 29,33g
=> Mg(24) và Ca(40)

\(a,\)Đặt CT chung của 2 KL là M
\(n_{H_2}=\dfrac{0,672}{22,4}=0,03(mol)\\ PTHH:M+2HCl\to MCl_2+H_2\\ \Rightarrow n_{M}=0,03(mol)\\ \Rightarrow M_{M}=\dfrac{1,67}{0,03}\approx 55,67(g/mol)\\\)
Vậy 2 KL cần tìm là Ca và Sr
\(b,\) Đặt \(\begin{cases} n_{Ca}=x(mol)\\ n_{Sr}=y(mol) \end{cases} \)
\(PTHH:Ca+2HCl\to CaCl_2+H_2\\ Sr+2HCl\to SrCl_2+H_2\\ \Rightarrow \begin{cases} 40x+88y=1,67\\ x+y=0,03 \end{cases} \Rightarrow \begin{cases} x\approx0,02\\ y\approx0,01 \end{cases}\\ \Rightarrow \begin{cases} m_{Ca}=0,02.40=0,8(g)\\ m_{Sr}=0,01.88=0,88(g) \end{cases} \)

a, Ta có: \(n_{H_2}=\dfrac{3,7185}{24,79}=0,15\left(mol\right)\)
Giả sử 2 KL cần tìm là A.
PT: \(A+2HCl\rightarrow ACl_2+H_2\)
Theo PT: \(n_A=n_{H_2}=0,15\left(mol\right)\)
\(\Rightarrow M_A=\dfrac{4,4}{0,15}=29,33\left(g/mol\right)\)
Mà: 2 KL nằm ở 2 chu kì kế tiếp.
→ Mg và Ca.
b, Ta có: 24nMg + 40nCa = 4,4 (1)
BT e, có: 2nMg + 2Ca = 0,15.2 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Mg}=0,1\left(mol\right)\\n_{Ca}=0,05\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Mg}=0,1.24=2,4\left(g\right)\\m_{Ca}=0,05.40=2\left(g\right)\end{matrix}\right.\)

Đáp án B.
Gọi công thức chung của hai kim loại là X
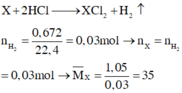
Mà hai kim loại ở 2 chu kỳ liên tiếp thuộc nhóm IIA → 2 kim loại đó là Ca và Mg




Gọi kim loại trung bình là R
R + 2HCl → RCl2 + H2 ↑
Ta có: nR = nH2 =0, 672 : 22,4 = 0,03 mol
Suy ra MR = mR : nR =0, 88 : 0,03 = 29,33 (g/mol)
Mà hỗn hợp gồm hai kim loại kiềm thổ ở hai chu kì liên tiếp nên 2 kim loại đó là Mg (M=24) và Ca (M=40).
a, Gọi 2 kim loại là \(\overline{X}\)
\(\overline{X}+HCl\rightarrow XCl_2+H_2\)
\(n_{H2}=\frac{0,672}{22,4}=0,03\left(mol\right)\)
\(n_{\overline{X}}=\frac{0,88}{X}\left(mol\right)\)
\(n_{\overline{X}}=n_{H2}\Rightarrow\frac{0,88}{\overline{X}}=0,03\)
\(\Rightarrow0,03\overline{X}=0,88\Rightarrow\overline{X}=29,33\)
\(24< \overline{X}< 40\)
Vậy 2 kim loại lần lượt là Mg,Ca
b, \(Mg+2HCl\rightarrow MgCl_2+H_2\)
__a______________________a__
\(Ca+2HCl\rightarrow CaCl_2+H_2\)
b_____________________b
Giải hệ phương trình :
\(\left\{{}\begin{matrix}24a+40b=0,08\\a+=0,03\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,02\\b=0,01\end{matrix}\right.\)
\(\Rightarrow m_{Mg}=0,02.24=0,48\left(g\right)\)
\(\Rightarrow\%_{Mg}=\frac{0,48}{0,88}.100\%=54,55\%\)
\(\Rightarrow\%_{Ca}=100\%-55,54\%=45,45\%\)