Bài 1:Nung 400g CaCO3, một thời gian thu được 312g chất rắn.Tính H phản ứng
Bài 2:Nung 200g CaCO3 một thời gian với H=75% thu được chất rắn A. Để hòa tan hoàn toàn A cần x(g) dd HCl 14.6%, sau phản ứng thu được khí B và dd D
a) Tính thể tích khí B thu được( đktc )
b) Tìm x
c) Tính C% của dd D
Giúp mình với mọi người owiiiii <3
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1) \(m_{CO_2}=m_{rắn\left(trcpư\right)}-m_{rắn\left(saupư\right)}=100-64,8=35,2\left(g\right)\)
=> \(n_{CO_2}=\dfrac{35,2}{44}=0,8\left(mol\right)\)
=> \(V_{CO_2}=0,8.22,4=17,92\left(l\right)\)
2)
PTHH: CaCO3 --to--> CaO + CO2
0,8<---------0,8<---0,8
=> \(m_{CaCO_3\left(pư\right)}=0,8.100=80\left(g\right)\)
3)
\(m_{CaCO_3\left(bd\right)}=\dfrac{100.90}{100}=90\left(g\right)\)
=> Rắn sau pư chứa CaCO3, CaO, tạp chất
\(m_{tạp.chất}=100-90=10\left(g\right)\)
\(m_{CaCO_3\left(saupư\right)}=90-80=10\left(g\right)\)
\(m_{CaO}=0,8.56=44,8\left(g\right)\)
\(1,n_{CaCO_3}=\dfrac{90\%.100}{100}=0,9\left(mol\right)\\ PTHH:CaCO_3\rightarrow\left(t^o\right)CaO+CO_2\\ Đặt:n_{CaCO_3\left(p.ứ\right)}=a\left(mol\right)\left(a>0\right)\\ Ta.có:m_{rắn}=64,8\left(g\right)\\ \Leftrightarrow10+\left(90-100a\right)+56a=64,8\\ \Leftrightarrow a=0,8\left(mol\right)\\ n_{CO_2}=n_{CaO}=n_{CaCO_3\left(p.ứ\right)}=0,8\left(mol\right)\\ V_{CO_2\left(đktc\right)}=0,8.22,4=17,92\left(l\right)\\ 2,m_{CaCO_3\left(p.ứ\right)}=0,8.100=80\left(g\right)\\ 3,Rắn.sau.nung:m_{tạp.chất}=10\%.100=10\left(g\right)\\ m_{CaO}=0,8.56=44,8\left(g\right)\\ m_{CaCO_3\left(dư\right)}=\left(0,9-0,8\right).100=10\left(g\right)\)

Không biết đúng hay sai nữa , có sai thì cầu mong thứ tha ![]()
Theo đề bài ta có : \(\left\{{}\begin{matrix}nCO2=\dfrac{0,672}{22,4}=0,03\left(mol\right)\\nHNO3=0,5.0,2=0,1\left(mol\right)\end{matrix}\right.\)
Ta có PTHH :
(1) \(CaCO3-^{t0}\rightarrow CaO+CO2\)
0,03mol..................0,03mol...0,03mol
(2) \(CaO+2HNO3\rightarrow Ca\left(NO3\right)2+H2O\)
0,05mol.........0,1mol
Theo PTHH 1 và 2 ta có :
nCaO còn dư 0,02 (mol)
=> \(H=\dfrac{n_{\left(ch\text{ất}-thi\text{ếu}\right)}}{n_{\left(ch\text{ất}-d\text{ư}\right)}}.100\%=\dfrac{0,03}{0,05}.100\%=60\%\)
Vậy................


1) \(n_{O_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
mA = mKMnO4(bđ) - mO2 = 79 - 0,15.32 = 74,2 (g)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,3<-----------0,15<----0,15<---0,15
=> \(H=\dfrac{0,3.158}{79}.100\%=60\%\)
2)
\(\left\{{}\begin{matrix}\%m_{K_2MnO_4}=\dfrac{0,15.197}{74,2}.100\%=39,825\%\\\%m_{MnO_2}=\dfrac{0,15.87}{74,2}.100\%=17,588\%\\\%m_{KMnO_4\left(không.pư\right)}=\dfrac{79-0,3.158}{74,2}.100\%=42,587\%\end{matrix}\right.\)
3) \(n_{KMnO_4\left(không.pư\right)}=\dfrac{79}{158}-0,3=0,2\left(mol\right)\)
PTHH: 2KMnO4 + 16HCl --> 2KCl + 2MnCl2 + 5Cl2 + 8H2O
0,2----------------------------------->0,5
K2MnO4 + 8HCl --> 2KCl + MnCl2 + 2Cl2 + 4H2O
0,15-------------------------------->0,3
MnO2 + 4Hcl --> MnCl2 + Cl2 + 2H2O
0,15------------------->0,15
=> \(V_{Cl_2}=22,4\left(0,5+0,3+0,15\right)=21,28\left(l\right)\)
\(n_{KMnO_4}=\dfrac{79}{158}=0,5mol\)
\(n_{O_2}=\dfrac{3,36}{22,4}=0,15mol\)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
0,5 0,15
a)\(m_{KMnO_4}=0,15\cdot197=29,55g\)
\(m_{MnO_2}=0,15\cdot87=13,05g\)
\(m_{CRắn}=m_{KMnO_4}+m_{MnO_2}=29,55+13,05=42,6g\)
\(n_{KMnO_4pư}=0,15\cdot2=0,3mol\)
\(H=\dfrac{0,3}{0,5}\cdot100\%=60\%\)
b)\(m_{O_2}=0,15\cdot32=4,8g\)
\(\%m_{K_2MnO_4}=\dfrac{29,55}{42,6}\cdot100\%=69,37\%\)
\(\%m_{MnO_2}=100\%-69,37\%=30,63\%\)

nHCl=0,6 mol
FeO+2HCl-->FeCl2+ H2O
x mol x mol
Fe2O3+6HCl-->2FeCl3+3H2O
x mol 2x mol
72x+160x=11,6 =>x=0,05 mol
A/ CFeCl2=0,05/0,3=1/6 M
CFeCl3=0,1/0,3=1/3 M
CHCl du=(0,6-0,4)/0,3=2/3 M
B/
NaOH+ HCl-->NaCl+H2O
0,2 0,2
2NaOH+FeCl2-->2NaCl+Fe(OH)2
0,1 0,05
3NaOH+FeCl3-->3NaCl+Fe(OH)3
0,3 0,1
nNaOH=0,6
CNaOH=0,6/1,5=0,4M

a) \(n_{KCl}=\dfrac{14,9}{74,5}=0,2\left(mol\right)\)
PTHH: 2KClO3 --to--> 2KCl + 3O2
0,2<-----------0,2----->0,3
=> mKClO3 = 0,2.122,5 = 24,5(g)
VO2 = 0,3.22,4 = 6,72(l)
b) \(n_{KClO_3}=\dfrac{25,725}{122,5}=0,21\left(mol\right)\)
Gọi số mol KClO3 pư là a
=> (0,21-a).122,5 + 74,5a = 16,125
=> a = 0,2 (mol)
=> nO2 = 0,3 (mol)
=> VO2 = 0,3.22,4 = 6,72(l)
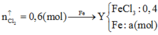
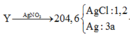
CaCO3-> CaO +CO2
nCaCO3=200/100=2 (mol)
nCaO=nCaCO3=2 (mol)
khối lượng CaO sinh ra : mCaO = 2*56=112(g)
khối lượng CaCO3 dư : m CaCO3 dư= 134-112=22(g)
khối lương CaCO3 phản ứng : mCaCO3 pư= 200-22=178(g)
Hiệu suất H=178/200 *100%=89%
Bài 1 :
\(m_{giam}=m_{CO2}=400-312=88\left(g\right)\)
\(CaCO_3\underrightarrow{^{to}}CaO+CO_2\)
Theo lý thuyết ,
100g CaCO3 tạo 44g CO2
400g CaCO3 tạo 176g CO2
\(\Rightarrow H=\frac{88}{176}.100=50\%\)
Bài 2 :
a, \(n_{CaCO3}=2\left(mol\right)\)
\(H=75\%\Rightarrow\) Có 1,5mol CaCO3 phản ứng
\(CaCO_3\underrightarrow{^{to}}CaO+CO_2\)
1,5______1,5__________
A gồm 0,5mol CaCO3 ; 1,5mol CaO
\(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\)
0,5______1_________0,5______0,5_________
\(CaO+2HCl\rightarrow CaCl_2+H_2O\)
1,5_____3_______1,5__________
\(\Rightarrow V=11,2\left(l\right)\)
b, \(n_{HCl}=4\left(mol\right)\)
\(\Rightarrow x=4.36,5:14,6\%=1000\left(g\right)\)
c,\(\Sigma n_{CaCl2}=2\left(mol\right)\Rightarrow m_{CaCl2}=222\left(g\right)\)
\(m_{dd_{spu}}=m_{CaCO3}+m_{CaO}+1000-m_{CO_2}\)
\(=1112\left(g\right)\)
\(\Rightarrow C\%_{CaCl2}=\frac{222.100}{1112}=19,96\%\)