Phần 2:
Bài 2: Cacbon cháy trong bình đựng khí oxi tạo thành khí cacbonic. Viết
PTHH và tính khối lượng khí cacbonic sinh ra trong mỗi trường hợp sau:
a) Khi có 6,4 gam khí oxi tham gia phản ứng?
b) Khi đốt 6 gam cacbon trong bình đựng 19,2 gam khí oxi?
Bài 3: Khi đốt khí metan (CH 4 ); khí axetilen (C 2 H 2 ), rượu etylic (C 2 H 6 O) đều
cho sản phẩm là khí cacbonic và hơi nước. Hãy viết PTHH phản ứng cháy của
các phản ứng trên?
Bài 4: Tính lượng oxi cần dùng để đốt cháy hết:
a) 4,65 gam Photpho b) 6,75 gam bột nhôm
c) 0,336 lít khí hiđro (ở đktc)
Bài 5: Trong phòng thí nghiệm người ta điều chế oxit sắt từ Fe 3 O 4 bằng cách
dùng oxi oxi hóa sắt ở nhiệt độ cao. Tính số gam sắt và thể tích oxi cần dùng
(ở đktc) để có thể điều chế được 6,96 gam oxit sắt từ?
Bài 7: Tính khối lượng oxi cần dùng để đốt cháy hoàn toàn 0,25 tấn than chứa
95% cacbon. Các tạp chất còn lại không cháy.
Bài 8: Viết những PTHH khi cho oxi tác dụng với:
a) Đơn chất: Zn, Fe, Na, S, Ba, K, Ca?
b) Hợp chất: CO, CH 4 , C 2 H 6 O, C 4 H 10 , C 3 H 7 OH.
Bài 9: Hãy giải thích vì sao:
a) Than cháy trong oxi tạo ra nhiệt độ cao hơn khi than cháy trong không khí?
b) Dây sắt nóng đỏ cháy sáng trong oxi, nhưng không cháy được trong không
khí?

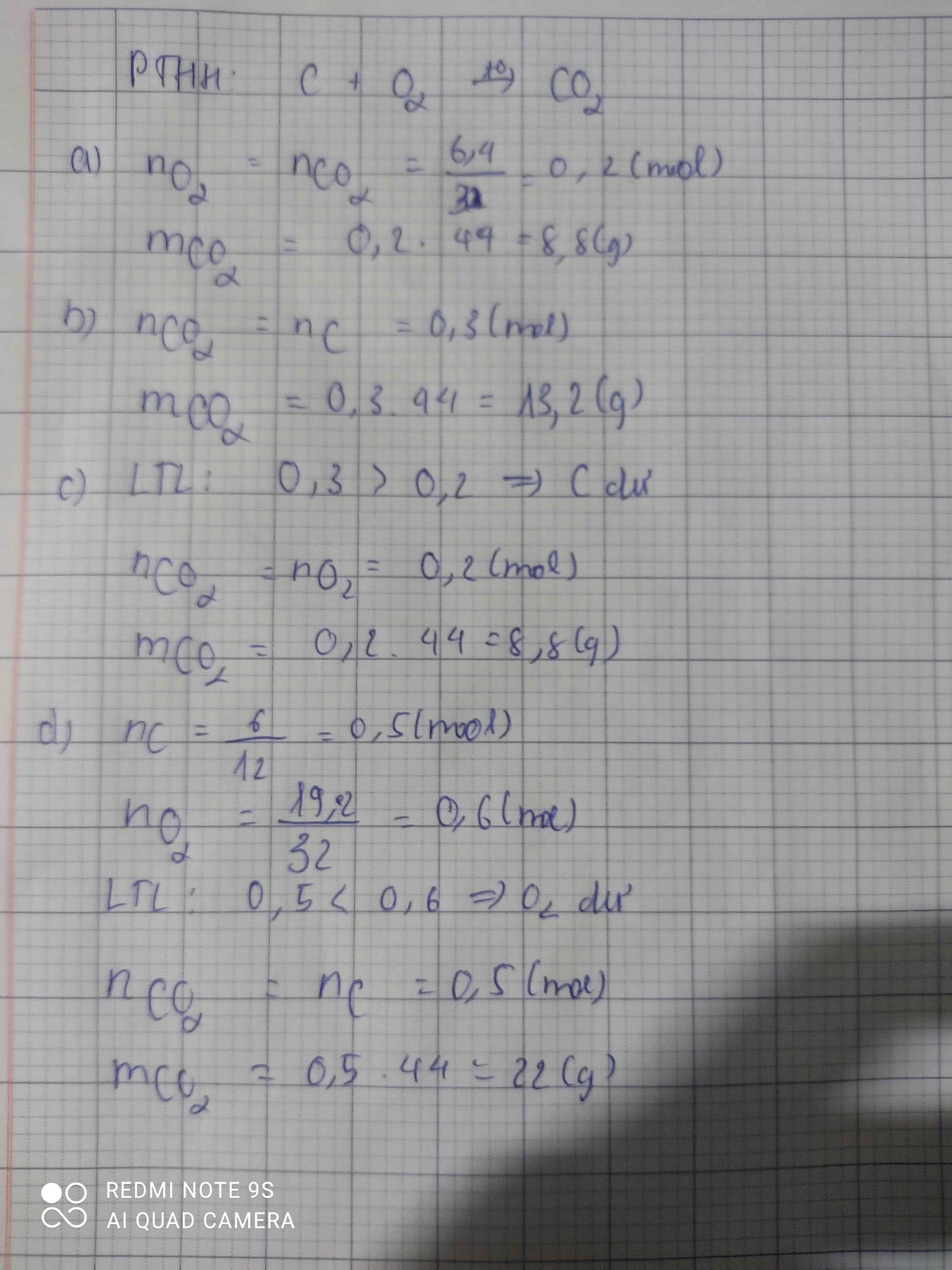
Bài 2:
\(C+O_2--to->CO_2\)
0,2_______________0,2
a) \(n_{O_2}=\frac{6,4}{32}=0,2\left(mol\right)\)
\(m_{CO_2}=0,2.44=8,8\left(g\right)\)
b) \(n_C=\frac{6}{12}=0,5\left(mol\right)\)
\(n_{O_2}=\frac{19,2}{32}=0,6\left(mol\right)\)
Theo pt :
\(n_{O_2}=n_C=0,5< 0,6\left(mol\right)\Rightarrow O_2\)dư
\(\Rightarrow n_{CO_2}=n_C=0,5\left(mol\right)\)
\(\Rightarrow m_{CO_2}=0,5.44=22\left(g\right)\)