Câu 1: Cho 2,7 gam Al phản ứng với 200ml dd FeSO4 1M. Sau khi phản ứng xảy ra hoàn toàn, cho biết.
A. Chất nào hết, chất nào dư?
b. Tính khối lượng Fe thu được (giả sử toàn bộ lượng Fe thu được đều bám trên thanh Al)
c. Dung dịch sau phản ứng gồm những chất nào. Tính nồng độ từng chất trong dung dịch.
Giúp mình với! cảm ơn rất nhiều




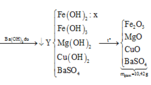
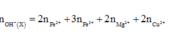

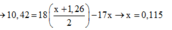
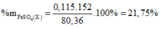

a) 2Al+3FeSO4--->Al2(SO4)3+3Fe
n Al=2,7/27=0,1(mol)
n FeSO4=1.0,2=0,2(mol)
0,1/2 < 0,2/3
--> FeSO4 dư
b) n Fe=3/2n Al=0,15(mol)
m Fe=0,15.56=8,4(g)
c) dd sau pư gồm FeSO4 và Al2(SO4)3
n FeSO4=3/2n Fe=0,15(mol)
n FeSO4 dư=0,2-0,15=0,05(mol)
CM FeSO4=0,05/0,2=0,25(M)
n Al2(SO4)3=1/2n Al=0,05(MOL)
CM Al2(SO4)3=0,05/0,2=0,15(M)
\(n_{Al}=\frac{2,7}{27}=0,1\left(mol\right)\)
\(n_{FeSO4}=1.0,2=0,2\left(mol\right)\)
a.\(PTHH:2Al+3FeSO_4\rightarrow Al_2\left(SO_4\right)_3+3Fe\)
Trước____ 0,1_____0,2_____________
Phản ứng___0,1___0,15_________
Sau____ 0______0,05 _________0,05 _____0,15
Nên Al hết và FeSO4 dư
b. \(m_{Fe}=0,15.56=8,4\left(g\right)\)
c. Dung dịch sau phản ứng gồm Al2(SO4)3 tạo thành và FeSo4 còn dư