Dẫn V lít khí hiđro (đktc) đi qua ống đựng 32 gam Fe2O3 nung nóng, phản ứng xảy ra vừa đủ, thu được m gam kim loại sắt và nước.a. Viết phương trình hóa học.b. Tính các giá trị V và m.c. m gam kim loại sắt thu được ở trên có tan hết trong dung dịch có chứa 0,6 mol axit sunfuric H2SO4 không? Biết Sắt tác dụng với axit sunfuric thu được sắt (II) sunfat và khí hidro.Biết Fe=56, H=1, O=16, S=32.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, PTHH:
Fe2O3 + 3H2 ---to---> 2Fe + 3H2O (1)
CuO + H2 ---to---> Cu + H2O (2)
b, nFe = \(\dfrac{2,8}{56}=0,05\left(mol\right)\)
nCu = \(\dfrac{6-2,8}{64}=0,05\left(mol\right)\)
Theo pt (1): nH2 (1) = 2nFe = 2 . 0,05 = 0,1 (mol)
Theo pt (2): nH2 (2) = nCu = 0,05 (mol)
=> VH2 = (0,1 + 0,05) . 22,4 = 3,36 (l)
c, Theo pt (1): nCuO = nCu = 0,05 (mol)
Theo pt (2): nFe2O3 = \(\dfrac{1}{2}n_{Fe}=\dfrac{1}{2}.0,05=0,025\left(mol\right)\)
=> m = 0,05 . 80 + 0,025 . 160 = 8 (g)
\(a.CuO+H_2-^{t^o}\rightarrow Cu+H_2O\\ Fe_2O_3+3H_2-^{t^o}\rightarrow2Fe+3H_2O\\ b.m_{Cu}=6-2,8=3,2\left(g\right)\\ n_{Cu}=0,05\left(mol\right);n_{Fe}=0,05\left(mol\right)\\ \Sigma n_{H_2}=n_{Cu}+\dfrac{3}{2}n_{Fe}=0,125\left(mol\right)\\ \Rightarrow V_{H_2}=2,8\left(l\right)\\ c.n_{CuO}=n_{Cu}=0,05\left(mol\right);n_{Fe_2O_3}=\dfrac{1}{2}n_{Fe}=0,025\left(mol\right)\\ m_{hh}=m_{CuO}+m_{Fe_2O_3}=0,05.80+0,025.160=8g\)

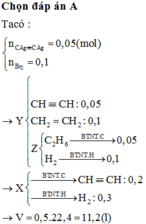
Đáp án A
● Cách 1: Tính toán theo phương trình phản ứng
Theo giả thiết, suy ra : Y gồm C 2 H 2 , C 2 H 4 , C 2 H 6 và có thể có H 2 . Z có C 2 H 6 và có thể có H 2 .
Dựa vào số mol của các chất Br2, C2Ag2, CO 2 , H 2 O và bản chất phản ứng, ta có :
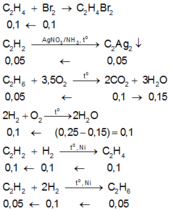
Suy ra :
n H 2 trong X = 0 , 3 ; n C 2 H 2 trong X = 0 , 2 V X đktc = V C 2 H 2 + V H 2 = 11 , 2 lít
● Cách 2: Sử dụng phương pháp bảo toàn nguyên tố
Theo giả thiết, suy ra :
n C 2 H 2 dư = n C 2 Ag 2 = 0 , 05 ; n C 2 H 4 = n Br 2 = 0 , 1 ; n H 2 O = 0 , 25
Nhận xét : Các chất trong X đều chứa 2 nguyên tử H. Mặt khác, số mol của C 2 H 2 dư, C 2 H 4 và H 2 O đều đã biết. Vậy áp dụng bảo toàn nguyên tố H là tính được số mol của hỗn hợp X. Vì thế không mất nhiều thời gian viết phương trình phản ứng và tính toán như cách 1.
Áp dụng bảo toàn nguyên tố đối với H, ta có :
2 n H 2 + n C 2 H 2 ⏟ n X = 2 n C 2 H 2 dư ⏟ 0 , 05 + 4 n C 2 H 4 ⏟ 0 , 1 + 2 n H 2 O ⏟ 0 , 25 ⇒ n X = 0 , 5 mol ⇒ V X đktc = 11 , 2 lít
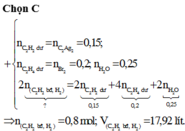
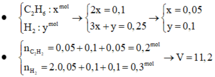

n Fe2O3=32/160=0.2 (mol)
a) PTHH:
Fe2O3+3H2-> 2Fe+3H2O (1)
0.2----->0.6___0.4__0.6___(mol)
b) V=V H2=0.6*22.4=13.44(l)
m=m Fe= 0.4*56=22.4 (g)
c)
Fe+H2SO4-> FeSO4+H2 (2)
(2)=> n Fe = n H2SO4
Mà theo bài ra, n Fe = 0.4 mol < n H2SO4 = 0.5=6 mol
Suy ra: m gam kim loại sắt thu được ở trên tan hết trong dd có chứa 0.6 mol axit sunfuric H2SO4