Một muối ngậm nước có công thức là CaSO4.nH2O. Biết 19,11g mẫu chất có chứa 4g nước. Hãy xác định công thức phương trình của muối ngậm nước trên
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

mCaSO4=19,11-4=15,11g
=>nCaSO4=15,11/136(mol)
nH2O=4/18 (mol)
Công thức là CaSO4:nH2O
=>1:n=nCaSO4:nH2O=1:2
=> CaSO4.2H2O

Theo đầu bài ta có tỷ lệ :
\(\dfrac{M_{CaSO4.nH2O}}{m_{CaSO4.nH2O}}=\dfrac{M_{H2O}}{m_{H2O}}=\dfrac{136+18n}{19,11}=\dfrac{18n}{4}\)
=> 544 + 72n = 343,98n
=> n = 2
Vậy công thức hóa học của muối là CaSO4.2H2O

a) \(\%Mg=\dfrac{24}{24+2.M_X+18n}.100\%=11,82\%\)
=> MX + 9n = 89,523
Xét n = 5 => MX = 44,5 (Loại)
Xét n = 6 => MX = 35,5 => X là Cl
Xét n = 7 => MX = 26,5 (Loại)
Xét n = 8 => MX = 17,5 (loại)
Vậy CTHH của tinh thể là MgCl2.6H2O
b) \(\%Cl=\dfrac{35,5.2}{203}.100\%=34,975\%\)
c) \(n_{MgCl_2.6H_2O}=\dfrac{40,6}{203}=0,02\left(mol\right)\)
=> nH = 0,02.12 = 0,24 (mol)
=> \(n_{H_3PO_4}=\dfrac{0,24}{3}=0,08\left(mol\right)\)
=> mH3PO4 = 0,08.98 = 7,84 (g)

có mFe/Mx=0.20144
\(\Rightarrow\) Mx=278 rồi tính được n=7
ct FeSO4.7H20

Đặt CTPT của muối cacbonat ngậm nước là:

Vậy CTPT của muối cacbonat ngậm nước là Na 2 CO 3 . H 2 O
Đáp án: A

Gọi công thức muối ngậm nước có dạng: RSO 4 . nH 2 O
Theo đề bài ta có hệ phương trình:
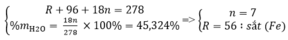
Vậy công thức của muối sắt là: FeSO 4 . 7 H 2 O
Cứ 136 + 18n (g) CaSO4.nH2O thì có 18n (g) H2O
Mà 19,11g CaSO4.nH2O có 4g H2O
=> \(\frac{136+18n}{19,11}=\frac{18n}{4}\)
=> 72n + 544= 343,98n
=> n=2
=>CTHH: CaSO4.2H2O