Cho 15,92g hỗn hợp NaX và NaY (X, Y là các halogen ở hai chu kì liên tiếp nhau) vào dung dịch AgNO³ dư thì thu được 28,67g kết tủa. Xác định công thức 2 muối NaX và NaY.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A.
Hỗn hợp (NaX, NaY) = NaM
NaM + AgNO3 → AgM↓+NaNO3
Ta có
![]() => M = 81,6 => X,Y lần lượt là Br (80) và I (127)
=> M = 81,6 => X,Y lần lượt là Br (80) và I (127)

TH1: NaF và NaCl
Kết tủa chỉ có AgCl
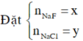
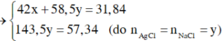
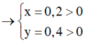
Vậy CT 2 muối có thể là NaF và NaCl
TH2: Hỗn hợp muối không chứa NaF
Đặt CT chung của 2 muối ban đầu là NaX
![]()
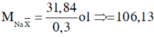
=> 2 muối là NaBr và NaI
Đáp án A

Cái chỗ M đó suy ra là \(M_X< 83,13< M_Y\)
Thì có 2 chất liên tiếp là Br (80) và I (127)

\(NaM+AgNO_3\rightarrow AgM+NaNO_3\)
\(n_{NaM}=n_{AgM}\)
\(\Leftrightarrow\frac{15,92}{23+M_M}=\frac{28,67}{108+M_M}\)
\(\Rightarrow M_M=83,333\)
\(\Rightarrow\) X là Brom(Br) ;Y là Iot(I)
Vậy NaX là NaBr và NaY là NaI

Đáp án C
Gọi công thức chung của NaX và NaY là NaM.
NaM + AgNO3 → AgM↓+NaNO3
0,03 →0,03 (mol)
![]()
=> M = 50,3 => X,Y lần lượt là Cl và Br

Gọi CT chung của 2 muối là NaZ.
Ta có: \(n_{NaZ}=\dfrac{31,84}{23+M_Z}\left(mol\right)\)
\(n_{AgZ}=\dfrac{57,34}{108+M_Z}\left(mol\right)\)
BTNT Z, có: \(n_{NaZ}=n_{AgZ}\Rightarrow\dfrac{31,84}{23+M_Z}=\dfrac{57,34}{108+M_Z}\)
\(\Rightarrow M_Z\approx83,133\left(g/mol\right)\)
Mà: X, Y thuộc 2 chu kì kế tiếp của nhóm VIIA.
→ Br, I

Chọn A
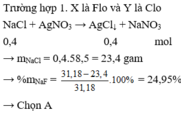
Chú ý: Với đề trắc nghiệm chọn được đáp án A có thể không cần xét thêm trường hợp 2.
Trường hợp 2. X khác Flo. Gọi hỗn hợp (NaX, NaY) tương đương với NaM


Gọi công thức chung là NaR
\(NaR+AgNO_3\rightarrow AgR+NaNO_3\)
\(n_{AgR}=\frac{28,67}{108+R}\)
\(n_{NaR}=\frac{15,92}{23+R}\)
Ta có :nAgR=nNaR
\(\Leftrightarrow\frac{15,92}{23+R}=\frac{28,67}{108+R}\)
\(\rightarrow R=83,13\)
\(\rightarrow Al\left(Br\right)< R< A_2\left(I_2\right)\)
\(\rightarrow NaBr,NaI\)