1. Hỗn hợp X gồm CuSO4 ; FeSO4 và Fe(SO4)3 có chứa \(\frac{64}{3}\)% theo khối lượng nguyên tố lưu huỳnh. Lấy 60 gam hỗn hợp X hòa tan hoàn toàn trong nước, sau đó thêm dung dịch NaOH(loãng) cho đến dư. Phản ứng hóa học xong, lọc lấy kết tủa đem nung ngoài không khí tới khi khối lượng chất rắn không thay đổi, được hỗn hợp Y. Dẫn một luồng khí CO (dư) đi chậm qua Y (nung nóng) cho đến khi phản ứng xảy ra hoàn toàn, được m gam chất rắn Z.
a) Viết tất cả các phương trình phản ứng xảy ra.
b) Tính m (gam) ?
2. Trộn lẫn 100 ml dung dịch HCl a M với 250 ml dung dịch KOH b M, được dung dịch. KOH b M, được dung dịch X. Lập biểu thức toàn học thể hiện mối quan hệ giữa a và b, biết dung dịch X hòa tan vừa hết 9,75 gam nhôm hiđroxit.

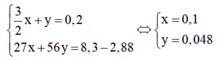

2. Trộn lẫn 100 ml dung dịch HCl a M với 250 ml dung dịch KOH b M, được dung dịch. KOH b M, được dung dịch X. Lập biểu thức toàn học thể hiện mối quan hệ giữa a và b, biết dung dịch X hòa tan vừa hết 9,75 gam nhôm hiđroxit.
______________________________
nAl(OH)3=\(\frac{7,75}{78}\)=0,125
nHCl=0,1a; nKOH=0,25b
HCl+KOH\(\rightarrow\)KCl+H2O
TH1: HCL hết
Ta có HCl+KOH\(\rightarrow\)KCl+H2O
______ 0,1a__0,1a
\(\rightarrow\)nKOH dư=0,25b-0,1a
Ta có Al(OH)3+KOH\(\rightarrow\)KAlO2+2H2O
nAl(OH)3=nKOH=0,25b-0,1a=0,125
\(\rightarrow\)0,25b-0,1a=0,125
TH2: KOH hết
Ta có HCl+KOH\(\rightarrow\)KCl+H2O
____0,25b__0,25b
\(\rightarrow\)nHCl dư=0,1a-0,25b
Ta có Al(OH)3+3HCl\(\rightarrow\)Al(OH)3+3H2O
nHCl=3nAl(OH)3=0,1a-0,25b=3.0,125=0,375
\(\rightarrow\)0,1a-0,25b=0,375
1.
a.
CuSO4+2NaOH\(\rightarrow\)Cu(OH)2+Na2SO4
FeSO4+2NaOH\(\rightarrow\)Fe(OH)2+Na2SO4
Fe2(SO4)3+6NaOH\(\rightarrow\)2Fe(OH)3+3Na2SO4
Cu(OH)2\(\rightarrow\)CuO+H2O
4Fe(OH)2+O2\(\rightarrow\)2Fe2O3+4H2O
2Fe(OH)3\(\rightarrow\)Fe2O3+3H2O
CuO+CO\(\rightarrow\)Cu+CO2
Fe2O3+3CO\(\rightarrow\)2Fe+3CO2
b. Trong 60g X, mS=60.64/3%=12,8
\(\rightarrow\)nS=0,4=nSO4
\(\rightarrow\)mSO4=0,4.96=38,4
\(\rightarrow\)mFe+mCu=60-38,4=21,6
\(\rightarrow\)m=21,6