Cho 7,1 g hỗn hợp gồm 1 kim loại kiềm X, và 1 kim loại kiềm thổ Y tác dụng hết với dd HCl dư thu được 5,6 l khí (đktc) . Tìm X, Y ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
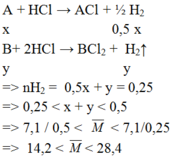
Chỉ có cặp nghiệm A = 23 (Na ) , B = 24 (Mg) thỏa mãn

X + HCl \(\rightarrow\) XCl + 1/2H2 (1)
Y + 2HCl \(\rightarrow\) YCl2 + H2 (2)
Gọi x, y tương ứng là số mol của X và Y, theo pt (1) và (2) ta có: x/2 + y = nH2 = 5,6/22,4 = 0,25 mol. Suy ra: x + 2y = 0,5. Như vậy: 0,25 < x + y < 0,5
Khối lượng nguyên tử trung bình của X và Y là: M = 7,1/(x+y) Suy ra: 14,2 < M < 28,4.
Do đó chỉ có trường hợp X là Na (23) và Y là Mg (24) có khối lượng nguyên tử trung bình phù hợp với trường hợp trên.

Cách khác :
Gọi số mol X, Y lần lượt là a, b
nhh = a + b (mol)
2X + 2HCl → 2XCl + H2↑
a__________________\(\frac{a}{2}\)
Y + 2HCl → YCl2 + H2↑
b__________________b
nH2 = 5,6 : 22,4 = 0,25 mol
→ a + 2b = 0,25 mol
\(\left\{{}\begin{matrix}a+b< a+2b\\a+2b< 2\left(a+b\right)\end{matrix}\right.\)
→0,125<a+b<0,25
\(\frac{7,1}{0,25}< \frac{7,1}{a+b}< \frac{7,1}{0,125}\)
→28,4<Mhh<56,8

Gọi kim loại kiềm thổ chung là R.
\(R+2HCl\rightarrow RCl_2+H_2\)
0,25 0,25
\(\Rightarrow M_R=\dfrac{8,15}{0,25}=32,6\)
\(\Rightarrow R_1< 32,6< R_2\)
Mà hai kim loại nằm ở 2 chu kì liên tiếp nên:
\(\left\{{}\begin{matrix}R_1:24\left(Mg\right)\\R_2:40\left(Ca\right)\end{matrix}\right.\)

\(X+2H_2O\rightarrow X\left(OH\right)_2+H_2\uparrow\\ X\left(OH\right)_2+2HCl\rightarrow XCl_2+2H_2O\\ n_{HCl}=\dfrac{14,6\%.50}{36,5}=0,2\left(mol\right)\\ \Rightarrow n_X=n_{X\left(OH\right)_2}=\dfrac{n_{HCl}}{2}=\dfrac{0,2}{2}=0,1\left(mol\right)\\ \Rightarrow M_X=\dfrac{2}{0,1}=20\left(\dfrac{g}{mol}\right)\\ Vì:M_X< M_{Mg}\left(20< 24\right)\Rightarrow M_A< M_X\\ \Rightarrow A:Beri\left(Be=9\right)\)
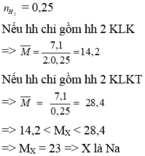

Chỉ có cặp nghiệm A = 23 (Na ) , B = 24 (Mg) thỏa mãn