Cho 1,9 g hỗn hợp muối cacbonat và hidrocacbonat của kim loại kiềm M tác dụng hết với dd HCl dư , sinh ra 0,448 l khí (đktc) .Tìm kim loại M ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chọn C.
Chọn D. Gọi CTPT : M2CO3; MHCO3
nCO2= nhh= 0,02 mol
→ M = 1,9/0,02 = 95 g
→ 17,5 < MM < 34 → M là Na.

Đáp án A
Đặt công thức muối cacbonat là M2CO3 có số mol x , muối hiđrocacbonat là MHCO3 có số mol y mol
M2CO3+ 2HCl → 2MCl + CO2+ H2O
x x mol
MHCO3+ HCl→ MCl + CO2+ H2O
y y mol
Ta có
n C O 2 = x+y= 0,448/22,4 = 0,02 mol = nhỗn hợp 2 muối
→ M h h ¯ = m h h n h h = 1 , 9 0 , 02 = 95
→ M+61< 95< 2M + 60 → 17,5<M<34 → Chỉ có Na thỏa mãn

Đáp án A
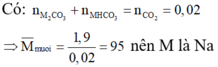
(Trong hỗn hợp cần có 1 muối có khối lượng mol lớn hơn và 1 muối có khối lượng mol < 95)

Gọi số mol của 2 muôi ban đầu lần lượt là \(x,y\) (mol).
Ta có: \(n_{CO_2}=\dfrac{0,448}{22,4}=0,02\left(mol\right)\)
PTHH: \(M_2CO_3+2HCl\rightarrow MCl+H_2O+CO_2\left(1\right)\)
Số mol: \(a\left(mol\right)\) ----------------------------------> \(a\left(mol\right)\)
\(MHCO_3+HCl\rightarrow MCl+H_2O+CO_2\left(2\right)\)
Số mol: \(b\left(mol\right)\) -------------------------------------> \(b\left(mol\right)\)
Theo (1) và (2), ta có:
\(n_{CO_2\left(1\right)}=n_{M_2CO_3}=a\left(mol\right)\); \(n_{CO_2\left(2\right)}=n_{MHCO_3}=b\left(mol\right)\)
\(\rightarrow n_{CO_2}=a+b=0,02\left(mol\right)\)
Có: \(\overline{M}_{M_2CO_3,MHCO_3}=\dfrac{1,9}{a+b}=\dfrac{1,9}{0,02}=95\)
\(\Leftrightarrow M+\left(1+12+16.3\right)< 95< 2M+\left(12+16.3\right)\)
\(\Leftrightarrow\dfrac{95-60}{2}< M< 95-61\Leftrightarrow17,5< M< 34\left(3\right)\)
Vậy chỉ có Natri (Na) là thỏa (3).

CTHH của 2 muối là M2CO3 và MHCO3 với số mol là a và b
\(\text{M2CO3 + 2HCL --> 2MCL + CO2 + H20}\)
\(\text{MHCO3 + HCl----> MCL + Co2 + H2O}\)
Ta có :
\(\text{nCO2 = a + b=0,02}\)
\(\text{(2M + 60) .a + (61+M).b=1,9}\)
Thử lần lượt các giá trị của M vào ta được
M=23 , a=b=0,01 mol
--->M là Na

Đặt công thức muối cacbonat là M2CO3 có số mol x , muối hiđrocacbonat là MHCO3 có số mol y mol
M2CO3+ 2HCl → 2MCl + CO2+ H2O
x x mol
MHCO3+ HCl→ MCl + CO2+ H2O
y y mol
Ta có: \(n_{CO_2}=x+y=0,25\left(mol\right)=n_{hh2muối}\)
=> \(\overline{M_{hh}}=\dfrac{30}{0,25}=120\left(g/mol\right)\)
Ta có: M+61< 120< 2M + 60
=> 30<M<59
=> Chỉ có Kali thỏa mãn
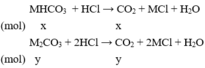
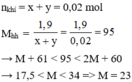

Công thức 2 muối: MHCO3; M2CO3
nCO2= 0,02 mol
Ta có:
M+61<\(\frac{1,9}{0,02}\)<2M+60
⇒ 17,5<M< 35
⇒ M là: Na