Cho Fe tan vừa hết trong H2SO4 thu được khí A( duy nhất) và 8,28g muối
a) Tính khối lượng Fe đã phản ứng. Biết rằng số mol Fe phản ứng bằng 37,5% số mol H2SO4
b) Dẫn toàn bộ khí A ở trên vào 100ml dd NaOH 1M . Tính nồng độ mol của dd sau phản ứng ( cho rằng thể tích dd không thay đổi)


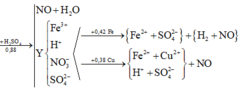


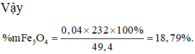

a.
2Fe + 6H2SO4 —> Fe2(SO4)3 + 3SO2 + 6H2O
2x 6x x 3x
Fe + Fe2(SO4)3 —> 3FeSO4
y y 3y
\(\rightarrow\) nFe = 2x + y = 37,5%.6x
m muối = 400(x - y) + 152 . 3y = 8,28
\(\rightarrow\) x = 0,02 và y = 0,005
\(\rightarrow\) nFe = 2x + y = 0,045
\(\rightarrow\)mFe = 2,52
b.
nNaOH = CM . V = 1 . 0,1 = 0,1 mol
nSO2 = 3x = 0,06mol
2NaOH + SO2 ---> Na2SO3 + H2O
0,1 0,05 0,05
Na2SO3 + SO2 + H2O ----> 2NaHSO3
0,01 0,01 0,02
\(\rightarrow\)dd sau phản ứng gồm: Na2SO3: 0,04mol và NaHSO3: 0,02mol
CM Na2SO3 = 0,04 : 0,1 = 0,4M
CM NaHSO3 = 0,02 : 0,1 = 0,2M
Tham khảo